Dr. Sergio Santana Porbén,1 Dr. Jesús Barreto Penié,2 Lic. Carmen Martínez González,3 Lic. Alicia Espinosa Borrás,3 Téc. Leydianna Morales Hernández 4
La evaluación del estado nutricional del paciente hospitalizado es parte
esencial de los programas de intervención alimentaria, nutrimental y
metabólica. La desnutrición hospitalaria es un hallazgo frecuente,
y la causa de costos incrementados de asistencia médica, alargamiento
de la estadía hospitalaria, y aumento de las tasas de morbilidad y mortalidad.
Los indicadores descritos en este artículo pueden obtenerse de forma
exacta y precisa, y permiten el monitoreo del progreso de la terapia nutricional.
Los perfiles nutricionales son una forma costoefectiva de integrar creadoramente
la información aportada por indicadores de diverso tipo en los cuidados
nutricionales del paciente hospitalizado. No obstante, la interpretación
correcta de los indicadores depende del contexto en que se empleen: pacientes
con enfermedades crónicas no transmisibles, en espera de cirugía
electiva,
críticos, sépticos, entre otros.
DeCS: Desnutrición Energético-Nutrimental / Evaluación
Nutricional /Perfil Nutricional / Índices Pronósticos.
La evaluación nutricional es un ejercicio clínico (esto es, al lado de la cama del paciente) en el que se reúnen indicadores de diversos tipos (antropométricos, bioquímicos, inmunológicos) con propósitos de diagnóstico, pronóstico y monitoreo:1
| ¿Está desnutrido el paciente? | Sí | No |
| En caso de respuesta positiva: ¿La desnutrición afecta el compartimiento proteico visceral? |
Sí | No |
|
¿El paciente se beneficiaría de un esquema de apoyo nutricional? |
Sí | No |
|
En caso de decidirse una conducta medicoquirúrgica: |
Sí Sí |
No No |
|
Una vez instalado el esquema de |
Sí | No |
La desnutrición como un desorden de la composición
corporal del paciente El cuerpo humano puede verse como la suma de 2 grandes
compartimientos: uno graso y otro magro.2 El
componente graso concentra el 85 % de la grasa corporal, y representa del 10
al 30 % del peso corporal, dependiendo del sexo. Cabe esperar que las mujeres
presenten un mayor porcentaje de grasa corporal que los hombres.
El compartimiento magro representa, tal vez, el compartimiento hístico
más importante de la economía, porque concentra la proteína
corporal, sustrato estructural de los tejidos activos metabólicamente.3
La proteína hística se distribuye, a su vez, en 2
compartimientos: uno somático y otro visceral. El compartimiento somático
está constituido por el tejido muscular esquelético (diafragma
y corazón incluidos), y aunque le corresponde el 30 % del peso corporal
del paciente, representa el componente principal de los tejidos metabólicamente
activos.4 El 75% del tejido muscular esquelético
se concentra en brazos y piernas.5
Por su parte, el compartimiento visceral está constituido por las vísceras
del tracto gastrointestinal, y los sistemas celulares
como la médula ósea y el tejido linfoide asociado al tubo digestivo,
entre otros tejidos. La unión de los compartimientos
somático y visceral origina la masa celular corporal.6
Se debe hacer notar que el 75 % del compartimiento magro está
constituido por el agua corporal total.2
La desnutrición produce cambios significativos de la composición
corporal del paciente.7 Aunque estos cambios
son pronunciados en el compartimiento graso, son aún más profundos
en el magro (y en especial, en la masa celular corporal): la
pérdida de más del 40 % de este compartimiento es incompatible
con la vida.8 La reducción del compartimiento
magro como consecuencia de la deprivación nutrimental crónica
y/o estados hipercatabólicos, indica la incapacidad creciente de la economía
para utilizar energía a fin de sostener las funciones vitales del organismo.9-10
Por ello, es necesario entender la desnutrición energéticonutrimental
como un desorden de la composición corporal del paciente:11
Los cambios en la composición corporal del paciente resultan
en desórdenes bioquímicos y clínicos que distorsionan la
respuesta normal del huésped frente a la enfermedad y su tratamiento.11
Se han propuesto numerosos indicadores del estado nutricional del ser humano. Puede mejorarse la utilidad diagnóstica de estos indicadores si se correlacionan con un componente particular de la composición corporal. En la tabla 1 de este artículo se presentan algunos de los más frecuentemente utilizados.
TABLA 1. Indicadores propuestos para inclusión en un perfil nutricional del sujeto humano
|
Compartimiento corporal de interés
|
Indicador
|
Punto de corte
|
Utilidad
|
|
Graso
|
Pliegues cutáneos
|
< p25
|
Diagnóstico Monitoreo a
mediano plazo |
|
Muscular
|
Circunferencia del brazo
|
< p25
|
Diagnóstico Monitoreo a mediano plazo
|
|
Excreción urinaria de creatinina
|
Índice de excreción
de creatinina < 80 % |
Diagnóstico Pronóstico
Monitoreo a corto plazo |
|
|
Visceral
|
Proteínas secretoras hepáticas
|
Albúmina
< 35 g/L |
Diagnóstico Pronóstico
Monitoreo a mediano plazo |
|
Conteo total de linfocitos
|
< 1500
células/mm 3 |
Diagnóstico Pronóstico
Monitoreo acorto plazo |
|
|
Excreción urinaria de nitrógeno
|
> 5 g/24 horas
|
Monitoreo a corto plazo
|
|
|
Suma de los compartimientos
|
Peso actual
|
Pérdida de
peso > 20 % |
Diagnóstico Pronóstico
Monitoreo |
|
|
Índice de masa corporal
|
< 18,5 kg/m 2
|
Diagnóstico Pronóstico
|
El peso actual es el indicador primario del estado nutricional
del paciente. Si se conoce que (aparte de las diferencias naturales determinadas
por el sexo), la grasa corporal representa entre el 25 y el 30 % del peso, y
el otro 30 % corresponde a la masa muscular esquelética, entonces una
reducción del peso del individuo puede interpretarse como una reducción
paralela de estos 2 compartimientos.7-9
La capacidad diagnóstica del peso actual como indicador del estado nutricional
del paciente puede mejorarse si se incorpora
a metámetros como el porcentaje de pérdida de peso y el índice
de masa corporal. Una pérdida de peso mayor del 20% respecto del peso
registrado 6 meses antes de la consulta o un Índice de masa corporal
inferior a 18,5 kg/m 2 son indicadores inequívocos para establecer el
diagnóstico de desnutrición.12-14
Ahora bien, la utilidad diagnóstica del peso actual puede estar influida
por el estado de hidratación del paciente. En particular, el peso actual
puede estar falsamente incrementado en pacientes con edemas y/o ascitis. Cambios
a corto plazo en el peso actual del paciente pueden reflejar cambios en la distribución
del agua entre los compartimientos intracelulares y extracelulares.
Aún así, en estos pacientes, el registro del peso actual informa
sobre cambios en el compartimiento del agua extracelular en
respuesta a la terapéutica médica.
La grasa subcutánea concentra del 50 al 60 % de la grasa
corporal. Por consiguiente, su medición pudiera servir para evaluar el
estado de preservación del compartimiento graso y por lo tanto, su reserva
energética. 15
La medición de los pliegues cutáneos grasos mediante un calibrador
dedicado es la técnica más extendida de estimación de la
grasa subcutánea corporal. 16. Así,
la observación de pliegues grasos disminuidos apunta hacia una reducción
del tamaño del compartimiento graso.
Asimismo, la medición de los pliegues grasos cutáneos es el punto
de partida para la construcción de modelos compartimentales de la composición
corporal (graso/no graso).2
A pesar de las ventajas señaladas, la imprecisión de la estimación
de la grasa corporal a partir de los pliegues grasos cutáneos depende
fuertemente del grado La desnutrición como un desorden de la composición
corporal del paciente El cuerpo humano puede verse como la suma de 2 grandes
compartimientos: uno graso y otro magro.2 El
componente graso de pericia y entrenamiento del personal técnico involucrado.17
Por otro lado, la utilidad diagnóstica de la medición de los pliegues
cutáneos depende del constraste del valor obtenido respecto a tablas
de referencia elaboradas con sujetos sanos dentro de la población de
pertenencia.
La circunferencia del brazo (CB) ha sido propuesta como un indicador
del estado de preservación del compartimiento muscular.18
Una CB disminuida se asocia fuertemente con una reducción del tamaño
del compartimiento muscular.19
La medición de la CB es una técnica sencilla y directa, y permite
conocer (en una primera aproximación) la integridad de la masa muscular
esquelética.
Si la CB se combina con los pliegues cutáneos, se pueden construir metámetros
(circunferencia muscular del brazo, áreas
muscular y grasa del brazo) valiosos para la realización de inferencias
adicionales sobre el estado de los compartimientos
muscular y graso.20
Las mediciones antropométricas pueden ser útiles en el diagnóstico
del estado nutricional del paciente. Sin embargo, su
insensibilidad ante cambios a corto plazo en los compartimientos corporales,
en particular después de la instalación de
esquemas de apoyo nutricional, las inutiliza para el monitoreo del estado nutricional
del paciente a corto plazo.
En virtud de que la creatinina se origina por hidrólisis
no enzimática de la creatina, y de que el 98 % de este compuesto se encuentra
en el músculo esquelético, entonces la medición de la creatinina
excretada en una colección de orina de 24 horas puede servir para hacer
inferencias sobre el tamaño del compartimiento muscular esquelético.21
La utilidad diagnóstica de la excreción urinaria de creatinina
mejora si se corrige para la excreción esperada del catabolito
en un sujeto que comparta la talla del paciente.22
Un índice de excreción de creatinina menor del 80 % puede predecir
una falla del paciente en el destete de un ventilador mecánico, o el
riesgo de aparición de una infección respiratoria.
A pesar de sus atractivos, la utilidad diagnóstica de la excreción
urinaria de creatinina está influida por factores preaanalíticos
muy difíciles de normalizar, como la recogida correcta de la colección
de orina de 24 horas,23 y la cuantía
del consumo de carnes rojas en la dieta regular del paciente.24
Además, la excreción urinaria de creatinina cuantifica químicamente
el tamaño del compartimiento muscular esquelético.25
Ello podría explicar la ausencia de correlación entre este indicador
y otros que expresan antropométricamente el tamaño del
compartimiento muscular esquelético (circunferencia del brazo, métodos
imagenológicos).
La medición de las concentraciones séricas de las
proteínas secretoras hepáticas puede servir para evaluar el estado
de la integridad y funcionalidad del compartimiento visceral.26
En efecto, la síntesis hepática de proteínas demanda de
la integridad de un pool de aminoácidos que se renueve continuamente
a partir de las proteínas ingeridas en la dieta regular del paciente:
una reducción en la cantidad y/o la calidad de las proteínas dietéticas
se traducen forzosamente en una disminución de la tasa de síntesis
de las proteínas secretoras hepáticas: albúmina, prealbúmina
y transferrina.27-28 Cabe esperar que, en la
misma medida en que se restablezca el aporte de proteínas, se incrementen
las concentraciones séricas de estos indicadores. La rapidez con la que
la tasa de síntesis de proteínas secretoras hepáticas refleje
los cambios en los ingresos proteicos será una función de la vida
media de las proteínas hepáticas.
La albúmina es el indicador de elección en la evaluación
de la integridad y la funcionalidad del compartimiento visceral: 1) una albúmina
disminuida, en un individuo con una historia de ingresos dietéticos subóptimos,
es suficiente para establecer el diagnóstico de la desnutrición;11
2) una albúmina disminuida es un predictor importante del riesgo del
paciente de complicarse
después de conducido el plan terapéutico, y del riesgo de fallecer
en caso de complicaciones.29-30
La prealbúmina ha sido otro de los indicadores de integridad del compartimiento
visceral que mayor interés ha recibido en años recientes.28
Un tiempo de vida media acortado, una composición aminoacídica
rica en triptófano y un menor tamaño del pool
hacen de la prealbúmina la nueva elección en la evaluación
de cambios en el tamaño del compartimiento visceral, en
respuesta a una terapia nutricional especificada.31
No obstante, la utilidad diagnóstica de las proteínas secretoras
hepáticas dependerá en gran medida de la fase clínica en
que
se encuentre el paciente en el momento del diagnóstico nutricional. En
casos de respuesta a la agresión, las proteínas secretoras hepáticas
se comportan como reactantes negativos de fase aguda, y su síntesis y
liberación se deprime, en favor de la producción de proteínas
de fase aguda como citoquinas, TNF y otras proteínas especializadas.32
También conspira contra la utilidad diagnóstica de las proteínas
secretoras hepáticas el tamaño del pool proteico (pooles de gran
tamaño se traducen en cifras séricas de la proteína insensibles
a cambios a corto y mediano plazo en la composición de los compartimientos
viscerales corporales después de instalada la terapia nutricional), la
distribución de la proteína entre los compartimientos extravascular
e intravascular (solo el 40 % de la albúmina se localiza en el compartimiento
intravascular), y la
preexistencia de enfermedad orgánica crónica (la síntesis
de proteínas secretoras hepáticas disminuye en casos de hepatopatías
crónicas; la concentración sérica de prealbúmina
se incrementa en casos de enfermedad renal crónica).32
No obstante, y a pesar de los inconvenientes apuntados, la determinación
de las proteínas secretoras hepáticas sigue siendo indispensable
en el diagnóstico de la desnutrición.26
TABLA 2. Proteínas secretoras hepáticas: Propiedades químicas y funciones.
|
Proteína |
PM
(kDa) |
Vida media |
Tamaño del pool |
Funciones
|
|
Albúmina |
68,0
|
18–20
|
3,5–5,0 g/Kg
|
Cadena polipeptídica única
entrecruzada por 17 puentes disulfuro La proteína circulante más abundante en el plasma y el líquido extracelular Proteína de transporte Sostenimiento de la presión oncótica del plasma |
|
Transferrina |
79,6
|
7–8
|
< 100 mg/kg
|
Cadena polipeptídica única |
|
Prealbúmina
|
55,0
|
1–2
|
10 mg/kg
|
Proteína tetramérica: las 4 subunidades
son idénticas entre sí y se disponen alrededor de un túnel
que en sus extremos presenta sendos sitios de unión para la tiroxina
Proteína transportadora de tiroxina Forma un complejo equimolecular con la proteína de unión al retinol: 50–70% de la prealbúmina se encuentra en forma de complejo prealbúmina-PUR Alto contenido en triptófano Pool de tamaño pequeño Sitio de degradación: riñón Sinonimia: Transtiretina TBPA (Thyroid-Binding-Prealbumin) |
|
Proteína de unión al
retinol |
21.0
|
0.5 – 1.0
|
2 mg/Kg
|
Transportadora de la forma alcohólica de la Vitamina
A
Sitio de degradación: riñón |
La respuesta inmune y el estado nutricional del paciente son entidades
inseparables: un paciente desnutrido se encuentra en riesgo incrementado de
sepsis debido a depresión del sistema inmune que acompaña a la
desnutrición.33 .Asimismo, un paciente
séptico está en riesgo de desnutrirse, debido a la cascada de
eventos metabólicos que desencadena la sepsis
(SIRS/FMO).33
El conteo total de linfocitos es un indicador inespecífico del estado
de inmunocompetencia del ser humano, y mide la capacidad del organismo de movilizar
células inmunoactivas para enfrentar la sepsis y la agresión.34
Un conteo total de linfocitos menor de 1 500 células/mm 3 puede alertar
al examinador de un riesgo incrementado del paciente de contraer una sepsis.35
La maquinaria metabólica celular es extremadamente lábil:
ante requerimientos energéticos incrementados y/o ingresos alimentarios
disminuidos, el organismo responde con un aumento en la movilización
de aminoácidos glucogénicos. El grupo amonio resultante de la
degradación aminoacídica se condensa en el hígado para
formar urea, la que, a su vez, se filtra libremente por el riñón.
Del 80 al 90 % del nitrógeno mensurable en la orina se corresponde con
la urea.26 Por lo tanto, la
determinación de la urea excretada en una colección de orina de
24 horas permite hacer inferencias sobre el estado del
equilibrio metabólico del paciente, y la manera en que responde a la
agresión (sepsis, injuria orgánica).36
De hecho, la
determinación del nitrógeno ureico puede ser tan útil como
la calorimetría indirecta en la estimación de las necesidades
energéticas y nutrimentales del sujeto hospitalizado. Además,
la determinación de nitrógeno ureico puede servir con
propósitos pronósticos: cambios en la situación clínica
del paciente se pueden anticipar por los cambios en la excreción
urinaria de nitrógeno ureico.
De la exposición anterior se comprende que el diagnóstico
de la desnutrición no depende del resultado de un solo indicador.
De hecho, si la condición nutricional de un paciente es descrita mediante
dos o más indicadores, cabe esperar que al menos uno de ellos caiga fuera
de los intervalos de referencia, sin que ello implique necesariamente que esté
afectado.37,38 A medida
que se incrementa el número de indicadores, el riesgo de clasificar incorrectamente
el estado nutricional del paciente aumenta
exponencialmente.39
Por lo tanto, el diagnóstico del estado nutricional debe establecerse
ante afectación de uno o más de los compartimientos corporales.
A modo de ejemplo, si ha ocurrido una reducción del peso corporal del
paciente, junto con una disminución de la circunferencia del brazo y
de los pliegues cutáneos, entonces se puede establecer la presencia de
una desnutrición tipo marasmo. La gravedad del desmedro nutricional puede
afirmarse de la concurrencia de dos o más indicadores nutricionales.
La afectación aislada de un indicador nutricional no implica forzosamente
un diagnóstico de desnutrición. De hecho, se
puede constatar una pérdida de peso mayor del 10 % en un paciente por
demás con pliegues cutáneos conservados y
Albúmina sérica =35,0 g/L.40 No obstante, en casos como estos
la mejor filosofía es denotar al paciente como de alto riesgo de desnutrición,
e iniciar el esquema de repleción nutricional pertinente.
Así mismo, la obtención de una albúmina sérica <
35,0 g/L no conduce automáticamente a denotar al paciente como desnutrido.
La hipoalbuminemia puede obedecer a trastornos de la síntesis hepática
de proteínas plasmáticas no relacionados con la ingestión
corriente de energía y/o proteínas (como puede ser el caso de
enfermedades hepáticas o renal crónicas), o a la presencia de
cuadros de respuesta a la agresión.26,32
No obstante, una hipoalbuminemia en un paciente crítico debe alertar
al equipo básico de trabajo de una respuesta incontrolada a la agresión
(estados posoperatorios complicados, sepsis, politraumatismos) para que inicie
las acciones necesarias para la solución de la agresión y la prevención
de afectaciones ulteriores de los tejidos magros.
TABLA 3. Proteínas secretoras hepáticas: proceder analítico, valores de referencia y valor de corte empleado en la evaluación nutricional del paciente.
|
Indicador
|
Proceder
|
Valores de
referencia (g/L) |
Valor de corte
(g/L) |
|
Albúmina
|
Colorimétrico:
Verde bromocresol Púrpura bromocresol |
35–55
|
26–31: depleción moderada
< 25: depleción grave |
|
Transferrina
|
Inmuno-nefelometría
|
> 2,0
|
1,0–1,5: depleción moderada
< 1,0: depleción grave |
|
Prealbúmina
|
Inmuno-nefelometría
|
> 0,2
|
0,05–0,1:
depleción moderada < 0,05: depleción grave |
|
Proteína de unión
al retinol |
HPLC
RIA EIA |
0,030–0,050
|
< 0.015: depleción grave
|
Se pueden aplicar técnicas estadísticas de análisis
multivariado para mejorar la efectividad del diagnóstico nutricional
del
paciente. Mediante estas técnicas se puede crear una función discriminante,41
una función de regresión múltiple,42-44
o
una función logística,45-46 que
devuelven cuán probable es que el paciente esté desnutrido si
ocurre una conjunción
particular de los indicadores nutricionales. En el caso clínico se presenta
una aplicación del índice de riesgo nutricional empleado en el
Estudio de Nutrición Parenteral Total de los Veteranos.47
TABLA 4. Diagnóstico nutricional: interrelación entre los valores de corte de los indicadores y las formas clínicas de la desnutrición.
|
Compartimiento corporal
|
Formas clínicas de la desnutrición
|
||
|
Deprivación energética (Tipo Marasmo)
|
Deprivación proteica
( Tipo Kwashiorkor) |
Formas mixtas
|
|
|
Graso
|
Pliegue cutáneo tricipital < p25
|
Pliegue cutáneo
tricipital =p25 |
Pliegue cutáneo
tricipital < p25 |
|
Muscular
|
Circunferencia del brazo < p25 1
|
Índice de excreción de
creatinina < 80 % |
Circunferencia del
brazo < p25 1 |
|
Índice de excreción de creatinina
< 80 % |
Circunferencia del brazo < p25 1
|
Índice de excreción de creatinina <
80 %
|
|
|
Visceral
|
Albúmina sérica =35 g/L
Conteo de linfocitos =1 500 células/mL |
Albúmina sérica < 35 g/L
Conteo de Linfocitos < 1 500 células/mL |
Albúmina sérica < 35 g/L Conteo de linfocitos < 1 500 células/mL |
|
Pérdida de peso > 10 % en los
últimos 6 meses |
Peso conservado
|
Pérdida de peso > 10 % en los
últimos 6 meses 2 |
|
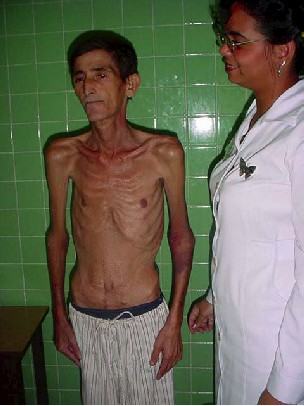
Paciente masculino de 47 años de edad, que en el año 2000 sufrió una resección intestinal masiva en el curso de una oclusión mecánica por bridas. El tránsito intestinal se resolvió mediante una yeyunotransversostomía. El paciente ha evolucionado con 7–15 diarreas líquidas diarias, trastornos hidroelectrolíticos y desequilibrios ácido-básicos que han resultado en ingresos hospitalarios frecuentes.
Fig.1. Caso clínico. Desnutrición energética nutrimental a tipo Mixta Grave. Se aprecia la ausencia de depósitos grasos subcutáneos y la depleción de los tejidos musculares.
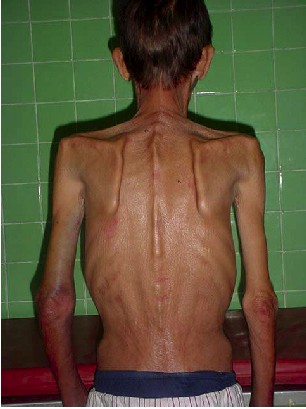
Fig.2. Caso clínico. Se aprecian las escápulas
aladas y las apófisis espinosas prominentes, debido a la reducción
notable de los depósitos grasos subcutáneos.
Acude ahora por debilidad, astenia, pérdida de peso y diarreas
crónicas.
Los resultados del perfil nutricional se exponen a continuación:
|
Compartimiento corporal
|
Indicador
|
Valor
|
Interpretación
|
|
Graso |
Pliegue
tricipital (mm) |
2,6
|
< p25 Grave
|
|
Muscular
|
Area grasa del
brazo |
1,8
|
< p25 Grave
|
|
Circunferencia
del brazo (cm) |
14,0
|
< p25 Grave
|
|
|
Circunferencia
muscular del brazo (cm) |
13,2
|
< p25 Grave
|
|
|
Área muscular
del brazo (cm 2 ) |
13,8
|
< p25 Grave
|
|
|
Índice de
excreción de creatinina (%) |
17,1
|
< 80.0 Grave
|
|
|
Visceral
|
Albúmina (g/L)
|
19,0
|
< 35.0 Grave
|
|
Suma de los
compartimientos |
Pérdida de peso
|
-48,0
|
> 10 % Grave
|
|
|
Índice de masa
corporal |
12,3
|
< 18.5 Grave
|
El diagnóstico de un cuadro grave de desnutrición
mixta se establece de la afectación universal de los compartimientos
corporales: graso, muscular, visceral.
El paciente fue clasificado como de alto riesgo nutricional mediante la función
desarrollada por Buzby y cols 47 (< 83,5).
The assessment of the nutritional status of the hospitalized patient is an
essential part of the metabolic, nutritional and feeding intervention programs.
Hospitalary malnutrition is a frequent finding, and the causes of increased
costs of medical care, augmented lengths of stay, and elevated morbidity and
mortality rates. The nutritional indicators described in this article can be
obtained accurately and precisely, and allow the monitoring of the progress
of the nutritional therapy. Nutritional profiles can be a cost-effective way
of creatively pooling the information brought about by indicators of varying
type in the nutritional care of the hospitalized patient. However, the correct
interpretation of the nutritional indicators depends upon the context where
they are to be used: patients with non-transmisible chronic diseases, those
waiting for elective surgery, critical patients, septic
ones, among others.
Subject headings: Energy Nutrient Malnutrition / Nutritional Assessment
/ Nutritional Profiles / Prognostic Indexes.
1 Especialista de II Grado en Bioquímica
Clínica. Diplomado en Nutrición Humana. Grupo de Apoyo Nutricional.
Hospital “Hermanos Ameijeiras”.
2 Especialista de II Grado en Medicina Interna. Máster en Nutrición
en Salud Pública. Instructor. Jefe del Grupo de Apoyo Nutricional. Hospital
“Hermanos Ameijeiras”.
3 Licenciada en Enfermería. Máster en Nutrición
en Salud Pública. Grupo de Apoyo Nutricional. Hospital “Hermanos
Ameijeiras”.
4 Técnica en Dietética. Miembro del Grupo de Apoyo Nutricional.
Hospital “Hermanos Ameijeiras”.