Descriptores DeCS: ANTIBIOTICOS/uso terapéutico; AGENTES ANTIINFECCIOSOS/uso terapéutico; ANTIBIOTICOS/historia; AGENTES INFECCIOSOS/historia; RESISTENCIA MICROBIANA A LAS DROGAS/fisiología; ANTIBIOTICOS/clasificación.
El desarrollo de la antibioticoterapia en la actualidad, permite un eficaz tratamiento de infecciones bacterianas agudas y algunas enfermedades crónicas, como la tuberculosis, pues los nuevos antibióticos resultan alentadores para el control de enfermedades virales e infecciones parasitarias y micóticas.
El desarrollo alcanzado por la microbiología en nuestros días, ha permitido identificar otros tipos de microorganismos e infecciones, por lo que se hace necesario el uso de nuevos fármacos para su tratamiento.
El empleo de agentes farmacológicos en el tratamiento de infecciones comienza cuando los chinos hace más de 2 500 años, utilizaron la cáscara enmohecida de la soja en el tratamiento de carbuncos, forúnculos e infecciones similares.1 En el año 1877 Pasteur y Joubert reconocen las potencialidades clínicas de los microorganismos como agentes terapéuticos.2 Ehrlich fue el primero en formular los principios de la toxicidad selectiva y en reconocer las relaciones químicas específicas entre los parásitos y los medicamentos, el desarrollo de resistencia a medicamentos en los parásitos y el papel de la terapéutica combinada para combatir dicha resistencia. Los experimentos de Ehrlich en la primera década de este siglo condujeron al descubrimiento de las arsfenaminas, primer triunfo importante de la quimioterapia planeada.2
La era moderna de la terapéutica antimicrobiana se inicia en 1934 con la descripción de Dogmak de la efectividad de la primera sulfonamida en el tratamiento de las infecciones experimentales por estreptococos.2
La llamada "Edad de Oro" de los antibióticos comienza en 1941 con la producción de la penicilina a gran escala y su utilización con buenos resultados en ensayos clínicos.1 En la actualidad se calcula que aproximadamente el 40 % de todos los pacientes hospitalizados reciben tratamiento con antimicrobianos, por lo que en la últimas décadas se han obtenido numerosos compuestos de esta índole, los que resultan de utilidad incuestionable, sin embargo, su amplio uso fomenta el aumento de la resistencia de los gérmenes, lo que crea una necesidad cada vez mayor de nuevas drogas, y se encarece el tratamiento.3-5 En este sentido, resulta imprescindible para nuestro trabajo diario, conocer los criterios farmacológicos y microbiológicos que permitan el uso más racional de estos compuestos.
Es propósito de este artículo esbozar los principios generales que rigen el uso de los agentes antimicrobianos específicamente los antibióticos.
Con frecuencia se han utilizado de manera indistinta los términos antibiótico, antimicrobiano y quimioterápico para designar sustancias químicas definidas con actividad contra microorganismos específicos, como ya señalamos, el antibiótico es una sustancia producida en la naturaleza por microorganismos vivos o sintetizada en el laboratorio, por lo que se considera un producto de la evolución y puede conferir una ventaja selectiva a quienes los producen en un ecosistema específico.
Desde el punto de vista técnico, los antibióticos difieren de los quimioterápicos en que estos últimos son productos de síntesis química, aunque algunos como las sulfonamidas tienen actividad antibacteriana, por lo que se ha propuesto el término Aantimicrobiano@ para describir a todas las sustancias con esta actividad, ya sean naturales o de origen sintético.7,8
Según el efecto que ejerzan sobre la bacteria pueden ser (tabla 1):
| Bactericidas | Bacteriostáticos |
| Penicilinas | Tetraciclinas |
| Cefalosporinas | Eritromicina |
| Aminoglucósidos | Sulfonamida |
| Rifampicina | Novobiocina |
| Quinolonas | Cloranfenicol |
| Monobactámicos | |
| Polimixinas |
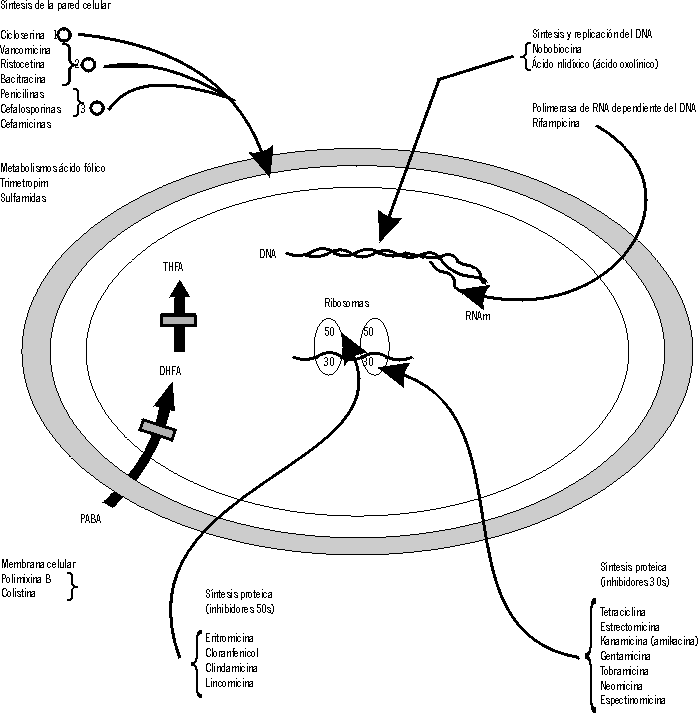
La clasificación que se basa en el mecanismo de acción de los antibióticos, resulta de gran utilidad, sobre todo si hay que utilizar simultáneamente varios agentes.
Según su mecanismo de acción, los antibióticos se clasifican como sigue (fig. 1, tabla 2):

TABLA 2. Clasificación de los antibióticos según su mecanismo de acción sobre la estructura bacteriana
| I. Inhibición de la síntesis de la pared celular | Penicilinas |
| Cefalosporinas | |
| Vancomicina | |
| Fosfomicina | |
| Tercoplanina | |
| Bacitracina | |
| II. Lesión en la permeabilidad de la membrana | Poliomixinas |
| celular | Colistinas |
| Nistatina | |
| Anfotericín B | |
| III. Inhibición de la síntesis proteica | Cloranfenicol |
| Tetraciclina | |
| Aminoglucósidos | |
| Lincomicinas | |
| Eritromicina | |
| IV. Inhibición de la síntesis de ácidos nucleicos | Quinolonas |
| Sulfonamidas | |
| Rifampicina | |
| Trimetropín |
Las bacterias son microorganismos hiperosmolares con respecto a los tejidos y al líquido intersticial de los mamíferos, por tanto, para mantener su integridad cuando infectan al hombre, necesitan una pared celular rígida.
La inhibición de la síntesis de la pared bacteriana tiene habitualmente un efecto bactericida.1 La estructura de la pared celular es un polímero denominado peptidoglicano, cuya síntesis se divide en 3 etapas principales, cada una de éstas es inhibida por un grupo de antibióticos diferentes.
En la primera etapa se forma el UDP-N-acetil-munamil-pentapéptido en el citoplasma bacteriano.2,6 En la segunda etapa, se polimerizan el UDP-N-acetil-muramil-pentepéptido y la N-acetilglucosamina que son transportados a través de la membrana citoplasmática y se unen al punto de crecimiento de la pared bacteriana. Esta fase es inhibida por antibióticos como la vancomicina y la bacitracina.6,7 Por último, las cadenas de peptidoglicano, una vez fuera de la célula, quedan entrelazadas transversalmente y dan lugar a la formación de un polímero tridimensional, esta etapa, también conocida como reacción de transpeptidación es inhibida por las penicilinas y las cefalosporinas.9-11
El ribosoma bacteriano más pequeño que el de los ma míferos, consta de 2 subunidades denominadas 50s y 30s; el antibiótico se une a los ribosomas bacterianos y bloquean la acción del RNA mensajero, este bloqueo en ocasiones es reversible. En el caso de los aminoglucósidos, éstos se unen a la subunidad ribosomal 30s y producen la acumulación de complejos iniciales de la síntesis proteica, lectura errónea del código RNAm y producción de poli péptidos anormales que se comportan como bactericidas.70
4. Inhibición de la síntesis de los ácidos nucleicos.
Las fluoroquinolonas, sulfonamidas, rifampicín, novobiocín y los nitroimidazoles actúan por este mecanismo al inhibir de forma selectiva, la enzima RNA polimerasa dependiente del DNA, lo cual cataliza la transcripción de la información genética contenida en el RNA mensajero y se convierte así en un potente bactericida.11,13,14
Mediante el método de tinción de Gram, las bacterias pueden clasificarse en grampositivas y gramnega tivas (tabla 3). La naturaleza química de la pared celular bacteriana permite regir sus propiedades de tinción, por lo que pueden dividirse las bacterias en dos subgrupos en dependencia de la coloración que adopte el microorganismo, al ponerse en contacto con determinados colorantes: aquéllos que retienen el colorante y permanecen de color azul después de ser tratados con alcohol, se clasifican como grampositivos; ejemplos de ellos son: el estafilococo, estreptococos, corynebacterium. Las bacterias que se decoloran completamente con el alcohol y después se colorean en rojo por la safranina, son identificadas como gramnegativas; ejemplos de ellas son: las Neisseria meningitidis y la Escherichia Coli.2,7,14
| Grampositivos | Gramnegativos |
| Staphylococcus aureus | Neisseria meningitidis |
| Streptococcus ß hemolíti- | |
| co (A,B,C,G) | Neisseria gonorrhoeae |
| Streptococcus Grupo viridans | Acinetobacter |
| Streptococcus bovis | Bordetella pertussis |
| Enterococcus | Brucella |
| Streptococcus pneumoniae | Campylobacter fetus |
| Bacillus anthracis | Escherichia coli |
| Corynebacterium diphteriae | Haemophilus influenzae |
| Listeria monocytogenes | Klebsiella pneumoniae |
| Legionella pneumophila | |
| Proteus mirabilis | |
| Pseudomonas aeruginosa | |
| Salmonella typhis | |
| Serratia marcescens | |
| Shigella | |
| Bacteroides fragilis | |
| Yersinia pestis |
| I. Penicilinas | I. Grupo Benzilpenicilinas | Penicilina procaína | |
| Penicilina benzatínica | |||
| Penicilina benetamine con clemizol | |||
| II. Grupo (se absorben por vía oral, parecidas al primer grupo) | Azidocillín | ||
| Fenoximetilpenicilina | |||
| Fenoxietilpenicilina | |||
| Fenoxipropilpenicilina | |||
| III. Grupo | A | Penicilinas isoxazólicas | |
| (Meticillín resistente) | Cloxacillín | ||
| Dicloxacillín | |||
| Flucloxacillín | |||
| Oxacillín | |||
| B | Meticillín | ||
| C | Nafcillín | ||
| IV. Grupo Penicilinas de amplio espectro | - Ampicillín | ||
| Hetacillín | |||
| Melampicillín | |||
| - Ésteres del Ampicillín | |||
| Bacampicilina | |||
| Levampicilina | |||
| Pivampicilina | |||
| Talompicilina | |||
| - Ampicillín como componente | |||
| Amoxacilina | |||
| Cicloxicilina | |||
| Epicilina | |||
| Mecilina | |||
| Pivmecilina | |||
| V. Grupo Penicilina activa contra | - Ureidopenicilina | ||
| Apalcilina | |||
| Pseudomonas aeruginosa | Azlocillina | ||
| Mezlocillina | |||
| Piperacillina | |||
| - Carboxipenicilina | |||
| Carbenicilina | |||
| Caxfecilian | |||
| Carindacilina | |||
| Ticarcilina | |||
| Sulbenicilina | |||
| VI. Grupo Penicilina resistente a los Temocilina | Foramidocilina | ||
| Betalactamasas | |||
| II. Cefalosporina (*) | I. Grupo | Cefazaflur (1ra G.) | |
| Cefazolina (1ra G.) | |||
| Ceforadine (1ra G.) | |||
| Ceftezole (1ra G.) | |||
| Cefasetrile (1ra G.) | |||
| Cefaloridine (1ra G.) | |||
| Cefalotina (1ra G.) | |||
| Cefaprín (1ra G.) | |||
| II. Grupo | Cefaclor (1ra G.) | ||
| Cefadroxil (1ra G.) | |||
| Cefatrizine (1ra G.) | |||
| Cefroxadine (1ra G.) | |||
| Cefalexín (1ra G.) | |||
| Cefaloglicín (1ra G.) | |||
| Cefaridine (1ra G.) | |||
| III. Grupo | Cefamandole (2da G.) | ||
| Cefbuperazone (2da G.) | |||
| Cefmetazole (2da G.) | |||
| Cefodizime (2da G.) | |||
| Cefonicid (2da G.) | |||
| Cefotetán (3ra G.) | |||
| Cefotiam (2da G.) | |||
| Cefoxitín (2da G.) | |||
| Cefuroxime (2da G.) | |||
| IV. Grupo | Cefepime (4ta G.) | ||
| Cefetamet (3ra G.) | |||
| Cefmenoxime (3ra G.) | |||
| Cefodizime (3ra G.) | |||
| Cefotaxime (3ra G.) | |||
| Cefpirome (4ta G.) | |||
| Cefpodoxime (3ra G.) | |||
| Ceftazidime (3ra G.) | |||
| Ceftizoxime (3ra G.) | |||
| Ceftriaxone (3ra G.) | |||
| Latamoxef (3ra G.) | |||
| V. Grupo | Cefixime (3ra G.) | ||
| Ceftibutén (3ra G.) | |||
| VI. Grupo | Cefoperzona (3ra G.) | ||
| Cefpimizole (3ra G.) | |||
| Cefpiramide (3ra G.) | |||
| Cefsulodín (3ra G.) | |||
| III Betalactámicos | Carbapenems | Imipenem | |
| Imipenem + Cilastatín | |||
| Meropenem | |||
| Thienamicim | |||
| Monobactámicos | Aztreonam | ||
| Carumonán | |||
| Tigemonán | |||
| Inhibidores de las betalactamasas | Amoxacilina + Ácido clavulánico | ||
| Ampicillín + Subbactom | |||
| Ticarcilina + Ácido clavu- | |||
| lánico | |||
| Piperacilina + Tazobactam | |||
| Ácido halopenicilínico | |||
| IV. Macrólidos | Azitromicina | ||
| Claritromicina | |||
| Eritromicina | |||
| Josamicina | |||
| Kitasamicina | |||
| Midecamicina | |||
| Miocamicina | |||
| Micinamicina | |||
| Oleandomicina | |||
| Rosaramicina | |||
| Roxitromicina | |||
| Spiramicina | |||
| V. Tetraciclinas | Clortetraciclina | ||
| Clomocicline | |||
| Demeclocicline | |||
| Doxicicline | |||
| Limecicline | |||
| Metacicline | |||
| Minocidine | |||
| Oxitetraciclina | |||
| Rolitetraciclina | |||
| Tetraciclina | |||
| VI. Cloranfenicol | Cloranfenicol | ||
| Tianfenicol | |||
| VII. Amminoglucósidos | Estreptomicina | ||
| Neomicina | |||
| Kanamicina | |||
| Gentamicina | |||
| Tobramicina | |||
| Amikacina | |||
| Dibekacina | |||
| Habekacina | |||
| Isapemacina | |||
| Kasugamicina | |||
| Netilmicina | |||
| Paramomicina | |||
| Spectinomicina | |||
| Trospectomicina | |||
| Dihidroestreptomicina | |||
| VIII. Sulfonamidas | Para usos generales (han disminuido su uso por altos efectos colaterales, el que más se emplea es la triplesulfa) | Sulfatiazol | |
| Sulfadiazine | |||
| Sulfadimidine B.P. | |||
| Triplesulfa | |||
| Sulfa con compuestos altamente solubles (alcanzan grandes concentraciones en orina, principal uso en tratamiento de infecciones urinarias) | Sulfafurazole | ||
| Sulfametizole | |||
| Sulfasonidine | |||
| Compuestos de baja solubilidad | Talilsulfatiazol | ||
| Succinilsulfatiazol | |||
| Sulfaguanidine | |||
| Sulfaloxante de Calcio | |||
| Compuestos de larga y media actividad | Sulfametoxazole | ||
| Sulfametoxipiridozine | |||
| Sulfadimetoxine | |||
| Sulfadoxine | |||
| Sulfametopiracine | |||
| Sulfonamidas tópicas | Sulfasolazine | ||
| Sulfadiazina de Plata | |||
| Mafenide | |||
| IX. Lincosamidas | Lincomicina | ||
| Clindamicina | |||
| X. Antibióticos péptidos | Ciclopéptidos | Bacitracina | |
| Gramicidina | |||
| Polimixina | Sulfato de colistina | ||
| Sulfometate de colistina | |||
| Polimixín B | |||
| Depsipéptidos | Pristinamicina | ||
| Glicopéptidos | Daptomicina | ||
| Telcoplamina | |||
| Vancomicina | |||
| XI. Metronidazole | Nitroimidazole y Nitrotiazoles | Metronidazol | |
| Omidazol | |||
| Tinidazol | |||
| Niridazol | |||
| XII. Quinolonas | 4 Quinolonas | Acrosoxacín | |
| Cinoxacín | |||
| Ácido nalidíxico | |||
| Ácido oxolínico | |||
| Ácido pipemídico | |||
| Fluoroquinolona | Amifloxacín | ||
| Ciprofloxacina | |||
| Difloxacina | |||
| Enoxicina | |||
| Fleroxacina | |||
| Flumequine | |||
| Lomefloxacina | |||
| Norfloxacina | |||
| Ofloxacina | |||
| Pefloxacina | |||
| Temafloxacina | |||
| XIII. Rifamicina | Rifabutín | ||
| Rifampicina | |||
| Rifampicina sódica | |||
| Rifapentine | |||
| Rifaximen | |||
| XIV. Agentes | Ácido paraminosalicílico | ||
| antimicobac- | Capreomicina | ||
| terias | Clofazimina | ||
| Dapsone | |||
| Etambutol | |||
| Etionamida | |||
| Isoniazida | |||
| Pirazinamida | |||
| Tiacetazona | |||
| Tiambutosine | |||
| Viomicina | |||
| XV. Diamino- | Diaminopirimidas en | Co-Trimazine | |
| pirimidinas | combinación con sulfa | Co-Trimoxazole | |
| Pirimetamine | |||
| Trimetropín | |||
| XVI. Agentes | Azoles | Fluconazol | |
| Antimicóticos | Itraconazol | ||
| Ketoconazol | |||
| Miconazol | |||
| Flucitosine, 5-Fluorocitosine | |||
| Griseofulvina | |||
| Macrólido poliénico | Anfotericín B | ||
| Otros Agentes | Terbinafine | ||
| XVII. Antivirales | Adamantanes | Amantadina | |
| Rimantadina | |||
| Isoprinosine | |||
| Interferones | Interferón | ||
| Nucleósidos | Aciclovir | ||
| Ganciclovir | |||
| Idoxuridine | |||
| Ribavirín | |||
| Trifluxidine | |||
| Vidaradine | |||
| Zidovudine | |||
| Compuestos en desarrollo con limitación clínica | - | Bezimidozole | |
| Hidoxibentilbenzimidozole | |||
| Enviroxine | |||
| - | Agentes Quelantes | ||
| B-Diketone | |||
| Ácido Fosfónico | |||
| Foscarnet | |||
| Ácido Fosfonacético | |||
| - | Agentes Inmunomoduladores | ||
| Imutiol | |||
| Thimopentín | |||
| - | Interferones inductores | ||
| Ampligen | |||
| Pirimidinones | |||
| - | Nucleósidos | ||
| Arabinósidos | |||
| Citarabine | |||
| Vidarabine monofosfato | |||
| Dideoxinucleósido análogo 2' 3' | |||
| Dideoxicitidine | |||
| 2' 3' Dideoxyinosine | |||
| 2' Deoxyribosides | |||
| E-5 (2-Bromovinyl) 2' -Deoxiciridine | |||
| - | Nucleósidos con sustitución del azúcar | ||
| Fluoroiodoaracitosine 2' Fluoro B5-Metilaran | |||
| - | Thiosemicarbazones | ||
| Methisazone | |||
| - | Agentes misceláneos | ||
| Rifabutín | |||
| Antiminiotungstate | |||
| Catanospermine | |||
| CD-4-análogo | |||
| Aliogopéptidos y péptido T | |||
| Sulfato de polisacárido | |||
II Grupo: Compuestos orales de moderada actividad antibacteriana de resistencia al stafilococo y moderada resistencia a algunas enterobacterias de betalactamasas.
III Grupo: Compuestos parenterales de moderada actividad antimi crobiana resistentes a un amplio rango de betalactamasas.
IV Grupo: Compuestos parenterales con una actividad antimicrobiana potente y resistencia a un amplio rango de betalactamasas.
V Grupo: Compuestos orales con una potente actividad antibac teriana y resistencia a un amplio rango de belactamasas.
VI Grupo: Compuestos parenterales con una moderada actividad ente robacterias, pero activas contra pseudomonas aeruginosa, con resistencia a un amplio rango de betalactamasas.
Prácticamente, todos los antibióticos desarrollan esta condición frente a los grampositivos, así por ejemplo, las quinolonas y los aminoglucósidos inducen un efecto posantibiótico, tanto para los grampositivos como para los gramnegativos.9,12,20
El efecto posantibiótico significa que aun cuando no se erradiquen los gérmenes, éstos no proliferan nuevamente durante varias horas después de exponerlos a una concentración por encima de la concentración mínima inhibidora. Se ha demostrado además que en la fase de exposición posantibiótica, los microorganismos son más sensibles a la destrucción por los leucocitos.6
Se entiende por resistencia, el mecanismo a través del cual, la bacteria puede disminuir o inactivar la acción de los agentes antimicrobianos.23
Debe tenerse en cuenta que si bien la resistencia mi crobiana y resistencia clínica (fracaso terapéutico) están íntimamente relacionados, no son la misma cosa: la primera se refiere a la respuesta que desarrollan los patógenos susceptibles a las diferentes concentraciones de antibióticos mientras que la segunda, se refiere a la ineficiencia terapéutica, aun cuando las concentraciones del antimicrobiano sean correctas: las mismas dependen de factores extrabacterianos (selección inadecuada del antibiótico) o del huésped (neutropenia, cuerpos extraños, etc.)22,24
La permeabilidad de la pared celular está determinada por la naturaleza de ésta. En las bacterias grampositivas, esta pared usualmente no es una barrera que impide la penetración de los antibióticos; sin embargo, en las gramnegativas, representa una barrera difícil de vencer y que varía según las diferentes especies; así por ejemplo, la pared celular es más permeable en algunas especies de Neisseria y H. influenzae, que la Escherichia coli, P. aeruginosa y Proteus indolpo sitivo.21
En la Escherichia coli y otras bacterias entéricas, una proteína específica (PORINS) impide la entrada de antibióticos hidrófilos con un peso molecular de hasta 650 daltons.21
Ejemplos de resistencia por disminución de la permeabilidad son la resistencia de los bacilos gramnegativos a la penicilina G, la eritromicina, la clindamicina y la vancomicina, así como la resistencia de los estreptococos, P. aeruginosa y otras bacterias anaerobias a los aminoglucósidos.21,25
Las betalactamasas representan un grupo diferente de enzimas producidas por gérmenes grampositivos, gramnegativos aerobios y anaerobios capaces de hidrolizar el anillo betalactámico e inactivar el antibiótico correspondiente.18,23
Abraham y Cham, en 1940, publicaron los primeros informes en relación con su mecanismo de acción. Se ha demostrado que constituye un factor importante de resistencia de gérmenes como Staphylococcus aureus, H. influenzae, N. gonorreae, Bacteroides fragilis y algunas enterobacterias.18,23,25
La información genética para la síntesis de estas enzimas puede estar contenida en un cromosoma o en un plásmido y su producción puede ser una característica del germen (tasa de producción constante), aunque también la misma puede ser inducida en presencia de un sustrato apropiado.21,22
Richmond y Sykes27 dividieron estas enzimas en 5 grupos (I B V) basados en el perfil de su sustrato y en la respuesta a los inhibidores enzimáticos. En la práctica los más importantes son los grupos I y III.
El grupo I es producido en una cantidad significativa en presencia del antibiótico, codificado por los genes del cromosoma y universalmente distribuidos entre las cepas de las enterobacterias; estas betalactamasas son las responsables de la resistencia de cepas de bacilos gramnegativos nosocomiales a las cefalosporinas.21,29,30 Las betalactamasas del grupo III son enzimas de un alto espectro activas contra penicilinas y cefalosporinas y casi siempre codificadas por plásmidos; este grupo incluye el TEM betalactamasa que se encuentra presente en las enterobacterias, H. influenzae y N. gonorreae.29
Entre las bacterias anaerobias que producen beta lactamasas merece citarse el Bacteroides fragilis, el cual produce una cefalosporinasa capaz de ser inactivada por el ácido clavulánico 21. Como se conoce el ácido clavulánico y el sulbactam son capaces de inhibir las betalactamasas, fundamentalmente, aquéllas mediadas por plásmidos cuando se combinan con algunos antibióticos, amoxicillín, ticarcilina, ampicillín y otros.21,25,28
Recientemente se han identificado algunas cepas de betalactamasas que pueden hidrolizar los nuevos betalactámicos; en este grupo se incluyen enzimas mediadas por plásmidos aislados de cepas de Klepsiella pneumonae que pueden hidrolizar la cefotaxina y otras cefalosporinas de tercera generación, así como el aztreonam 27,29,31 y enzimas mediadas por cromosomas presentes en cepas de xantomas ( pseudomonas ) maltophia, así como Enterobacter cloacae, Serratia marcense y Bacteroides fragilis, capaces de hidrolizar el imipenem y el meropenem. 29
La tolerancia, si bien no es considerada propiamente un mecanismo de resistencia, puede en la práctica comportarse como tal. La tolerancia se define como la existencia de una CBM muy superior a la CTM y se atribuye a la selección de mutantes deficientes en sistemas autolíticos. Probablemente, las dosis altas destinadas a conseguir niveles muy superiores a la CIM del microorganismo reduzcan la selección de estas subpoblaciones, por lo que, cuando se sospecha la existencia de ésta es necesario prolongar el tiempo de duración del tratamiento.8,18
Los aspectos más importantes a tener en cuenta a la hora de seleccionar el antibiótico adecuado son:
En las situaciones en que sea posible, podemos auxiliarnos de pruebas simples como la tinción de Gram, la cual puede brindar una orientación inicial para la selección del antibiótico; hacemos énfasis en este proceder de fácil realización, bajo costo y probada confiabilidad, el cual con frecuencia no es utilizado.6,25 Otras técnicas y procederes con las que se pueden identificar el germen se describen con precisión en esta publicación en el capítulo correspondiente.
Existen algunas características del huésped que deben tenerse en cuenta a la hora de elegir el antibiótico.
La edad es un factor fundamental, puesto que las edades límites plantean situaciones particulares, así por ejemplo en los individuos de la tercera edad, las infecciones sobre todo bacterianas son muy graves y se complican con frecuencia; además, en este grupo el diagnóstico de infección bacteriana puede ser más difícil que en el adulto joven y no debe olvidarse a la hora de iniciar la terapéutica, que la toxicidad particular de algunos antibióticos puede ser más elevada en el anciano, ejemplo de esto son la nefrotoxicidad y ototoxicidad de los aminoglucósidos y el aumento de riesgo de la sobrecarga de volumen al emplear antibióticos que contienen abundante sodio (ticarcilina, carbamicina).18,32
Las alteraciones genéticas y del metabolismo pueden interferir en los efectos terapéuticos de algunos antibióticos. El déficit de glucosa G fosfato deshidrogenasa, puede condicionar la aparición de episodios de hemólisis ante una situación de sobrecarga oxidativa en individuos sometidos a tratamiento con cloranfenicol y sulfamidas.6 Se conoce que en pacientes diabéticos a los cuales se asocia una vasculopatía no es recomendable utilizar la vía intramuscular para administrar antibióticos, sobre todo si la terapéutica debe prolongarse por más de 7 días, además, se ha comprobado que algunos antibióticos como el cloranfenicol pueden potenciar el efecto de los hipoglicemiantes orales.8,14
Hay infecciones donde la penetración del antibiótico al foco séptico es dudosa y aunque los gérmenes proliferan a una velocidad menor, se hacen mas difíciles de destruir, tal es el caso de las endocarditis bacterianas y las osteomielitis.9,25
En las infecciones relacionadas con obstrucción de vías urinarias, respiratorias o biliares, la penetración antimicrobiana a estas zonas es pobre, lo que sucede también en presencia de cuerpos extraños (sondas, válvulas protésicas) y abscesos donde las bacterias proliferan lentamente y el antibiótico puede ser destruido por enzimas elaboradas por los microorganismos.9,33
El paso de un medicamento al LCR no sólo se relaciona con el fármaco en sí, sino también con el grado de inflamación meníngea. Los compuestos liposolubles como el cloranfenicol, isoniacida, rifampicina, sulfonamidas y metronidazol llegan bien al LCR. Los aminoglucósidos, anfotericina B y polimixinas, no se difunden en LCR aun cuando hay inflamación. Las cefalosporinas, vancomicina y tetraciclina tienen una buena difusión solamente en presencia de inflamación meníngea (fig. 2).
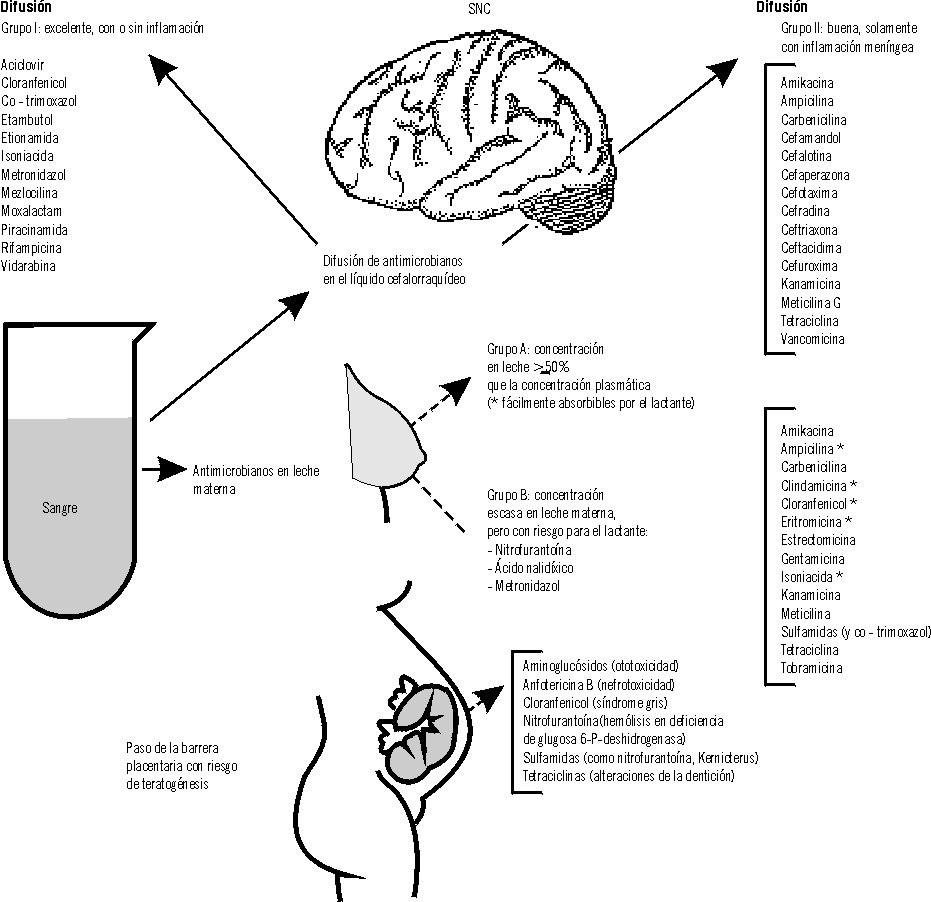
Prácticamente todos los antibióticos atraviesan la barrera placentaria, por lo que deben administrarse con mucha precaución durante el embarazo y la lactancia. La figura 2 ilustra las complicaciones que producen los diferentes antimicrobianos al pasar la barrera placentaria o excretarse por la leche materna.
Cuando los mecanismos de defensa del huésped están índemnes, la respuesta al tratamiento antimicrobiano es la misma, independientemente de que el antibiótico usado tenga actividad bactericida o bacteriostática,6,9 en caso de existir trastornos en dichos mecanismos, el control de la sepsis depende en gran medida del tipo de actividad antimicrobiana.18
En enfermedades tales como la drepanocitemia, neoplasias, diabetes mellitus, alcoholismo, trasplantes de órganos, síndrome de inmunodeficiencia adquirida, etc. la sepsis es un hecho temido y esperado de extraordinaria gravedad, además, estos enfermos en ocasiones son sometidos a antibioticoterapia profiláctica, que los predispone a superinfecciones con microorganismos resistentes y a sepsis nosocomiales de muy difícil control. Los gérmenes gramnegativos, los hongos, algunos protozoos (Pneumocystis carim) y algunos virus son los que infectan a estos pacientes con más frecuencia.35,36
Las alteraciones de la función renal y hepática influyen de manera decisiva sobre el empleo de estos fármacos. La mayoría de los antibióticos de uso común se eliminan sobre todo por el riñón; algunas excepciones incluyen la eritromicina y el cloranfenicol.18 Las concentraciones suelen ser más altas en orina y bilis que en suero, por lo que en la insuficiencia renal y hepática es necesario hacer ajustes posológicos.
En el riñón, los factores de los cuales depende la excreción del antibiótico son: el flujo sanguíneo renal, la filtración glomerular y el transporte transtubular, así por ejemplo los aminoglucósidos se eliminan por la filtración glomerular y las penicilinas por secreción tubular activa.8,18
Varios de los antibióticos de uso más frecuente, se metabolizan en el hígado y se excretan por la bilis; tal es el caso de las sulfonamidas, el cloranfenicol y la tetraciclina, por lo que debe también ajustarse la dosis o no administrarse cuando existe una hepatopatía aguda o crónica.19
La selección del antibiótico, las vías de administración y las dosis a utilizar están en dependencia también de la severidad de la infección del estado del enfermo. Se prefiere la vía parenteral para las sepsis graves, pacientes críticos cuando se requiere niveles terapéuticos del fármaco en sangre y tejidos profundos; también se prefiere la vía parenteral cuando la absorción oral o intramuscular es deficiente, también cuan do el tratamiento debe prolongarse más de 2 sema nas.15 En las tablas 5 y 6 se exponen los antibióticos que más se utilizan en la práctica diaria, así como sus dosis, vías de administración y gérmenes a los que son sensibles.
| Germen | Droga de 1ra opción | Alternativa terapéutica | También efectivos |
| I. Cocos y bacilos grampositivos | |||
| Staphilococcus aureus | |||
| a) Metilcillina sensible | PSRP (*) ej. Temocillín | Cefalosporinas de 1ra. G, vancomicina, eritromicina | Timentií, Unacyn, Imipenem, augmentín |
| Clindamicina | ciprofloxina pefloxacina | ||
| b) Meticillina resistente | Vancomicina | Tercoplanina | Ác. Fusídico, rifampicina, sulfaprim |
| - Staphilococcus epidermides | Vancomicina | PSRP | |
| - Streptococcus | Penicilina G-V | Betalactámicos, eritromicina | |
| A,B,C,G,F | |||
| - Streptococcus pheumoniae | Penicilina G | Múltiples drogas son efectivas, quinolonas, fluoroquilonas | Rifampicina + vancomicina |
| - Enterococcus | Penicilina G | Vancomicina + gentamicina | Ampicillina |
| Ampicillina + gentamicina | |||
| - Bacilos grampositivos | |||
| Bacilos anthracis | Ciprofloxacina o doxiciclina | Penicilina G, eritromicina | |
| Clostridium tetani | Metronidazol | Doxicilina | Imipenem |
| Clostridium perfringens | Clindamicina + penicilina G | Doxiciclina | Eritromicina, cloranfenicol, cefoxitina penicilinas antipseudomonas, imipenem |
| Clostridium difficile | Metronidazol (V.O.) | Vancomicina (V.O.) | Bacitracina (V.O.) |
| Corynebacterium diphteriae | Eritromicina | Penicilina G | Clindamicina, rifampicina |
| Listeria monocytogenes | Ampicillín | Sulfaprim | Eritromicina, penicilina G (alta dosis) |
| Aminoglucósidos antipseudomonas | |||
| II. Cocos y bacilos gramnegativos | |||
| - Neisseria meningitidis | Penicilina G | Ceftriaxone | Cefuroxima, cefotaxima, doxiciclina |
| Sulfonamidas (algunas cepas) | |||
| Cloranfenicol (profiláctico) | |||
| - Neisseria gonorrhoeae | Ceftriaxone, cefixime | Ofloxacina, ciprofloxacina, spectinomicina | Karamicina |
| - Bacilos gramnmegativos | Metronidazol | Clindamicina | Cefoxitina, imipenem, timentín |
| Bacteroides | Piperacilina B Tazobactan, unacyn | ||
| Enterobacter | Imipenem o penicilinas antipseudomonas + Aminoglucósidos antipseudomonas | + Timentín, ciprofloxacina | Cefalosporinas 4ta. G |
| Escherichia coli | Penicilinas + Inhibidores de | ||
| be+ talactamasas, Cefalosporinas | |||
| 3ra G, fluoroquinolonas | |||
| Sulfaprim, aminoglucósidos, nitrofurantoínas | |||
| Imipenem (dependiendo del sitio de infección) | |||
| Klebsiella pneumoneae | Cefalosporina 3ra G o ciprofloxacina | Aminoglucósidos antipseudomonas | Penicilinas antipseudomonas |
| Imipenem, aztreonam | |||
| Timentín, unacyn | |||
| Proteus mirabilis | Ampicillín | Sulfaprim | Augmentín, cefalosporinas 1ra., 2da, 3ra. G |
| Indol | Imipenem, aztreonam. | ||
| Proteus | |||
| Indol + (Providencia, Vulgari, Morganis) | Cefalosporinas 3ra G, fluoroquinolonas | Aminoglucósidos antipseudomonas | Imipenem, aztreonam |
| Providencia stuarti | Amikacina, ciprofloxacina, cefalosporinas 3ra G | Sulfaprim | Penicilinas antipseudomonas + amikacina |
| Imipenem | |||
| Salmonella typhi | Acitromicina, ceftriazone, cefoperazona | Cloranfenicol, amoxacillín, sulfaprim | - |
| Serratia marcescens | Amikacina, cefalosporinas | Aztreonam - | |
| 3ra G, imipenem, Fluoroquinolonas | |||
| Shigella | Fluoroquinolonas | Sulfaprim, ampicillín (resistente - en Latinoamerica y Medio Oriente) | |
| Yersinia enterocolítica | Cefalosporina 3ra G, Aminoglucósidos antipseudomonas | Ciprofloxacina | |
| Acinetobacter | Imipenem, fluoroquinolonas + amicacina Ceftaxidima | Se reporta 5 % resistencia a imipenem e incre mento de la resistencia a la amikacina y fluoroquinolonas | |
| Brucellas | Doxiciclina + gentamicina | Doxiciclina, sulfaprim, cloranfenicol | |
| Doxiciclina + rifampicina | |||
| Gardnerella vaginalis | Metronidazol | Clindamicina | |
| Haemophilus influenzae | |||
| - Meningitis | Cefotaxime | Sulfaprim | Cloranfenicol |
| Epiglotitis y otras infec- | Ceftriaxone | Imipenem | |
| ciones graves | Ciprofloxacina | ||
| Anpicillín (no productor de betalactamasas) | |||
| - Infecciones no graves | Argumentín, cefalosporinas orales de 2da y 3ra G | ||
| Sulfaprim, azitromicina, claritromicina, unacyn | |||
| Legionella pneumophila | Eritromicina + rifampicina | Azitromicina, claritromicina | Sulfaprim,pefloxacino, ciprofloxacino |
| - Otros gérmenes | |||
| Mycoplasmas pneumoniae | Eritromicina, azitromicina | Claritromicina | Doxicilina |
| Leptospira | Penicilina G, doxiciclina | - | - |
| Treponema pallidum | Penicilina G | Tetraciclina, eritromicina, cloranfenicol | - |
| Chlamydias pneumoneae | Doxiciclina | Eritromicina | Aztromicín, claritromicina |
| Chlamydias trachomatis | Acitromicina, doxiciclina | Ofloxacina, eritromicina | Ciprofloxacina |
| Citrobacter freundi | Imipenen | Fluoroquinolonas | Aminoglúsidos antipseudomonas |
| Pseudomona aeruginosa | Penicilinas antipseudomonas | Ciprofloxacino, cefalosporinas 4ta G timentín | - |
| Cefalosporinas 3ra G antipseudomonas, Imipenem, trobamicina | Aztreonan | ||
| Pseudomona cepacea | Sulfaprim, imipenem, ciprofloxacina | Minociclina, cloranfenicol | Habitualmente resistente a los aminoglucósidos |
| Vibrion cholerae | Doxiciclina, fluoroquinolonas | Sulfaprim | - |
| Campilobacter jejuni | Fluoroquinolonas | Eritromicina | Clindamicina, doxiciclina |
| Antimicrobianos | Dosis | Vías de administración | |
| Penicilinas 2da G | Nafcillín | 2 g c/4 h | ev |
| Penicilinas 3ra G | Unasyn (ampicillín +sulbactán) | 1,5 a 3g c/6 h | im-ev |
| Augmentín (amoxillina + ácido clavulánico) | 0,25 a 0,5 g c/8 h Oral | ||
| Penicilinas 4ta G | Ticarcillina | 3 g c/4 h | ev |
| Timetín (ticarcillina + ácido clavulánico) | 3,1 g c/4 a 6/h | im-ev | |
| Amdinocillín (Coactín) | 10 mg x kg c/6 h | im-ev | |
| Penicilinas 5ta G | Piperacillín | 3,4 g c/6 h | im-ev |
| Azlocillín | 3,4 g c/6h | im-ev | |
| Penicilinas 6ta. G | Temocillín | 1!2 g c 12 h | im-ev |
| Cefalosporinas 2da G | Cefoxitín (mefoxín) | 2 a 4 g c/8 h | im-ev |
| Cefomandole (mandol) | 2 g c/4 h | im-ev | |
| Cefalosporinas 3ra G. | Cefotaxime (clarofán) | 2 g c/4 h | im-ev |
| Ceftriazone (rocephín) | 1 g c/8 h | im-ev | |
| Ceftizoxime (cefizox) | 4 g c/8 h | im-ev | |
| Ceftazidime (Fortaz) | 1-2 g c/8 a 12 h | im-ev | |
| Cefalosporinas 4ta G. | Cefepime | 1-2 g c/8 h | im-ev |
| Aminoglucósidos | Amikacina | 15 mg x Kg x día (dosis única diluida o | im-ev |
| fraccionada en 2 dosis diarias) | |||
| Dibekacina | 1 mg x Kg c/8 a 12 h | im-ev | |
| Netilmicina | 4-7,5 mg x Kg x día c/8 a 12 h | im-ev | |
| Carbapenems | Imipenem!cilastin (primaxín) | 50 mg x Kg x día (dosis máxima) | ev |
| Meropenem | 1-2 g hasta 4 g diaria en 3 o 4 dosis) | ||
| Monobactámicos | Aztreonam (azactam) | 1-2 g c/6 a 8 h hasta 8 g | ev |
| Quinolonas | Ciprofloxacín | 500-750 mg c/12 h | Oral |
| 200-300 mg c/12 h | ev | ||
| Norfloxacín (noroxín) | 400 mg/día | Oral | |
| Enoxacín | 200-400 mg c/12 h | Oral |
Las manifestaciones de toxicidad más frecuentes de los antibióticos comúnmente utilizados, se resumen en la tabla 7.
| Antibióticos | Toxicidad | |
| I. | Penicilinas | Alergia-rash maculopapular, urticaria vesicular, dermatitis por contacto, eritema multiforme, síndrome Henoch-Schonlein, síndrome Stevens-Johnson, vasculitis. |
| Náuseas | ||
| Vómitos | ||
| Diarreas | ||
| Penicilina antiestafilococos | Nefrotoxicidad | |
| Nefritis intersticial | ||
| Fiebre, rash, hematuria y eosinofilia | ||
| Penicilina antipseudomonas | Diátesis plaquetaria | |
| II. | Cefalosporinas | Hipersensibilidad |
| Nefrotoxicidad | ||
| III. | Betalactámicos monobactámicos | Flebitis o molestias en el sitio de la infección |
| Alergia-erupción leve, náuseas, vómitos y diarreas | ||
| Incremento transitorio de los niveles de transaminasa y fosfatasa alcalina | ||
| Betalactámicos carbapenems | Convulsiones | |
| Náuseas | ||
| Vómitos | ||
| Diarreas | ||
| Alergia-erupciones | ||
| IV. | Macrólidos | Flebitis |
| Hepatitis colestásica (si se usa el estolato de eritromicina) | ||
| Fiebre medicamentosa | ||
| Exantemas | ||
| V. | Tetraciclinas | Hipersensibilidad |
| Fotosensibilidad | ||
| Hepatotoxicidad | ||
| Diabetes insípida renal (si se usa democlociclina) | ||
| Náuseas, vómitos | ||
| Papiledema en el adulto | ||
| VI. | Cloranfenicol | Depresión de la médula ósea |
| VII. | Aminoglucósidos | Ototoxicidad |
| Nefrotoxicidad | ||
| Bloqueo neuromuscular | ||
| Alergia (rash) | ||
| VIII. | Sulfonamidas | Hipersensibilidad |
| Necrólisis tóxica epidémica | ||
| Síndrome Steven-Johnson | ||
| Exacerba el lupus eritematoso sistémico | ||
| IX. | Lincosamidas | Enterocolitis seudomembranosa (por Clostridium difficile) |
| Anafilaxia | ||
| Leucopenia | ||
| X. | Antibióticos péptidos polimixinas | Parestesias |
| Bloqueo neuromuscular | ||
| Convulsiones | ||
| Antibióticos péptidos glicopéptidos | Hipersensibilidad | |
| Nefrotoxicidad | ||
| Hepatotoxicidad | ||
| Ototoxicidad | ||
| Hipotensión | ||
| XI. | Metronidazole | Hepatotoxicidad |
| Gusto metálico en la boca | ||
| Anorexia | ||
| Vómitos | ||
| Polineuritis | ||
| Crecimiento excesivo de candidas | ||
| XII. | Quinolonas | Náuseas |
| Vómitos | ||
| Convulsiones | ||
| Rash | ||
| Insomnio | ||
| Eleva enzimas hepáticas | ||
| Leucopenia y Neutropenia | ||
| Anemia | ||
| Toxicidad del SNC | ||
Se señala que durante el tratamiento antimicrobiano pueden presentarse sangramientos, los cuales se producen por diferentes mecanismos, tales como: interferencia con la vitamina K, trastornos de la función plaquetaria e hipoprotrombinemia.19 Los glicopéptidos, específicamente la tecloplamina puede producir un cuadro de trombocitopenia importante que desaparece cuando se suspende el tratamiento.37
Algunos antibióticos orales (cloranfenicol, tetraciclina, neomicín) deprimen la flora intestinal encargada de sintetizar la vitamina K, y pueden producirse sangramientos. El metronidazol y sus congéneres, cuando se administran conjuntamente con anticonceptivos orales, por un mecanismo de competencia desplazan en parte los derivados de cumarínicos fijados en la albúmina plasmática y pueden también provocar hemorragia.25
Un aspecto de suma importancia en el tratamiento, es el referido a los costos. Cualquier tratamiento con antibióticos de amplio espectro resulta extremadamente caro, pues a los mismos se le añaden además, los gastos de hospitalización; lo que obliga la aplicación de un ajuste racional, sin perjudicar la calidad de la atención médica.
Las ventajas y desventajas de las combinaciones de antibióticos y el uso profiláctico de la antibioticoterapia son aspectos polémicos. En el caso de las combinaciones, éstas tienen indicaciones precisas como son la bacteriemia polimicrobiana, pacientes críticos donde no se conoce el germen productor de la sepsis, infecciones nosocomiales graves y cuando es necesario reducir toxicidad y resistencia.25
Para la antibioticoterapia profiláctica deben preferirse antibióticos de bajo costo y toxicidad bien respaldados por una política antimicrobiana racional.
Subject headings: ANTIBIOTICS/therapeutics use; ANTI-INFECTIVE AGENT/therapeutic use; ANTIBIOTICS/history; ANTI-INFECTIVE AGENTS/history; MICROBIAN RESISTANCE TO DRUGS/physiology; ANTIBIOTICS/classification.
Dra. Lilliam Cordiés Jackson. Hospital Clinicoquirúrgico
"Hermanos Ameijeiras". San Lázaro No. 701 entre Belascoaín
y Marqués González, municipio Centro Habana, Ciudad de La
Habana, Cuba.
1 Especialista de II Grado en
Medicina Interna. Profesor Auxiliar.
2 Especialista de I Grado en Medicina Interna.
3 Especialista de I Grado en Neurofisiología.