Lic. Liena Roque Melgares,1 Dr C. Carmen M. Santos Hernández,2 Dr. Mario Hernández González 3 .
Justificación. La dieta ideal del paciente catabólico no está
bien definida. Aunque están disponibles muchas fórmulas nutricionales,
aún los investigadores trabajan en la búsqueda de una “dieta
diseñada a la medida”, que responda a las necesidades específicas
del paciente renal. Material y Método. Se realizó una investigación
prospectiva del balance metabólico y nutricional a 8 pacientes masculinos
con diagnóstico de insuficiencia renal crónica (IRC) terminal
durante tratamiento con
hemodiálisis (HD). Los pacientes fueron expuestos durante 12 semanas
a una intervención dietética que consistía en el registro
del consumo de alimentos mediante técnicas de recordatorio, y un menú
dirigido durante los 3 días semanales de diálisis. La dieta de
intervención fue confeccionada según los criterios de las XV Guías
Alimentarias de Asociación Norteamericana de Nefrología y los
comités de Expertos en Proteínas de FAO/OMS. Se analizaron las
variables dependientes: albúmina sérica, hemoglobina, bicarbonato,
ionograma, creatinina, urea y ácido úrico, así como el
índice de masa corporal y el diámetro vena cava por técnica
de ultrasonido. Los datos fueron analizados según la normalidad de las
variables, su distribución y sus medias. Se aplicaron la prueba t de
Student para muestras independientes, y un análisis de regresión
por pasos para las variables seleccionadas (SPSS versión 10, EEUU). Resultados.
Se demostró una asociación significativa entre la hemoglobina
y la
albúmina sérica con los ingresos de nitrógeno y sus cambios
en los días de diálisis durante las 12 semanas (test t de Student;
p < 0.05). La muestra de pacientes no presentó complicaciones durante
los 90 días del estudio y los ingresos de nitrógeno, histidina,
leucina, isoleucina y metionina, fueron controlados. Conclusiones. Se concluye
la importancia del uso de dietas a partir de alimentos naturales para el soporte
nutricional del paciente renal con su patrón específico de catabolismo
por su
bajo costo, factibilidad y aumento de la eficiencia metabólica en el
paciente renal.
DeCS: hemodiálisis / aminoácidos / eficiencia metabólica / patrón de catabolismo /dieta diseñada a la medida.
La insuficiencia renal crónica (IRC) consiste en la pérdida lenta
y progresiva, casi siempre irreversible, de las funciones
del riñón, a causa de enfermedades que producen una destrucción
bilateral difusa del parénquima renal y cuya expresión
clínica está dada por pérdida de las funciones renales.
A los pacientes que presentan esta enfermedad les es imprescindible la diálisis
como método depurativo que sustituye a los riñones en algunas
de sus funciones.
Por la importancia que reviste la Nutrición en la medicina clínica en las enfermedades prolongadas, como la IRC que suelen acompañarse de desnutrición,1 es válido destacar que el tratamiento nutricional constituye un aspecto esencial de la terapéutica de estos pacientes tratados en hemodiálisis, pues las consecuencias del estado urémico (anorexia, vómitos, náuseas), anormalidades endocrinas, pérdida de nutrientes durante la diálisis, bajo consumo de proteína dietética con o sin una adecuada ingesta energética, disminución de la palatabilidad de los alimentos debido a la restricción de sal, etc., pueden afectar el estado nutricional, incrementando la morbilidad y mortalidad.2-4
Por la importancia del tema, esta investigación se trazó como
objetivos: 1) Controlar la ingestión dietética de una muestra
de pacientes de insuficiencia renal (IRC) de la unidad de diálisis durante
12 semanas, evaluando macronutrientes y micronutrientes y una composición
aminoacídica de referencia para la histidina, isoleucina, leucina y metionina
para analizar su probable
asociación con la morbilidad y la mortalidad y la frecuencia de complicaciones
en el período de estudio; 2) estudiar la asociación de las variables
dietéticas con la evolución de las variables bioquímicas:
creatinina, urea, ácido úrico, ionograma, hemoglobina y albúmina
sérica; y 3) estudiar los cambios del índice de masa corporal
y el diámetro vena cava para precisar su probable asociación con
el ingreso hídrico y de nitrógeno.
Se seleccionaron 8 pacientes del sexo masculino de la unidad de Diálisis
del Centro de Investigaciones Médico-quirúrgico
(CIMEQ), quienes aceptaron voluntariamente participar en esta evaluación.
La edad promedio fue de 45 años y se consideró criterio de exclusión
la presencia de evidencias clínicas de enfermedad coronaria, hepática,
tiroidea o diabética. A los pacientes se les explicó el protocolo
de seguimiento y se obtuvo la correspondiente firma del acta de consentimiento.
A todos los pacientes se les efectuó una evaluación clínica mediante una historia clínica, examen físico y evaluación clínico nutricional. Los pacientes fueron seguidos durante 3 meses de intervención dietética con un control estricto del consumo de alimentos. Se calculó la dieta de intervención para los días de diálisis que permanecían en el hospital y los alimentos fueron pesados según técnicas cuantitativas, que consideran el peso en gramos de la oferta y los residuos dejados en cada plato.
A cada paciente se le suministró adicionalmente eritropoyetina, que previo al estudio no recibían, y además se garantizaba un ingreso de 35 mg de hierro oral por día. En los casos de ácido fólico y calcio también se garantizaba la satisfacción de las recomendaciones para la intervención a partir de la dieta y el suplemento.
Al finalizar los 3 meses de seguimiento a los pacientes en estudio se les repitieron las evaluaciones de las variables dependientes: albúmina sérica, hemoglobina, bicarbonato, monograma, creatinina, urea y ácido úrico, el índice de masa corporal y el diámetro vena cava por técnica de ultrasonido.
La ingesta de alimentos se evaluó por medio de encuestas dietéticas
que fueron realizadas durante el período interdiálisis y días
de hemodiálisis. En días interdiálisis se realizó
por el método retrospectivo de tipo recordatorio de un día. En
días de hemodiálisis se aplicaron métodos prospectivos
de tipo registro diario y peso directo de la oferta en bandeja y de los residuos
en el plato. El menú de intervención fue confeccionado según
los criterios de las XV Guías Alimentarias de la Asociación
Norteamericana de Nefrología y los comités de Expertos en Proteínas
de FAO/OMS, así como otras referencias.5-7
El control cuantitativo de los ingresos por día se procesó de forma computarizada.
Los nutrientes de interés para el estudio fueron: calorías, proteínas,
carbohidratos, lípidos, sodio, potasio, fósforo, magnesio,
líquidos, calcio, folatos, hierro, histidina, isoleucina, leucina, metionina
y nitrógeno.
La recomendación de la composición de aminoácidos de la
dieta de intervención durante los días de diálisis fue
considerada a partir de la referencia de la fórmula del Nefrosteril diseñada
por Fresenius Kabi (Alemania)8 . Se calcularon
los ingresos diarios de los aminoácidos (mg/g de proteína y g/día)
histidina, leucina, isoleucina y metionina para compararlos con valores
recomendados para población sana 9 y
con los recomendaciones para las personas con insuficiencia renal crónica
(IRC)10,11
Se establece como restricción para el ingreso hídrico, que la
misma no debiera ser mayor de 700 mililitros por día. Se
seleccionaron alimentos con alto contenido aminoacídico de histidina,
leucina, isoleucina y metionina.
A todos los pacientes se les realizó la pesada (en la silla pesa), se
les midió la estatura (en un antropómetro-estadiométrico)
y se realizó el cálculo correspondiente para determinar el índice
de masa corporal en los días 0 y 90 del tratamiento. Se realizó
la medición de la vena cava a través de un equipo de ultrasonido
en los días 0 y 90 del tratamiento.
Para el procesamiento y análisis estadístico de la información se empleó: promedio, medida de distribución, desviación estándar, prueba t de Student para muestras independientes y su análisis de probabilidad por coeficiente de Pearson, análisis de varianza y análisis de correlación y de regresión para las variables independientes: edad, peso, IMC, hemoglobina, albúmina sérica, sodio, potasio y bicarbonato del ionograma, creatinina, urea o ácido úrico.
El nivel de cumplimiento de los nutrientes evaluados en la dieta evolucionó favorablemente del período de pilotaje al período de intervención dietética, logrando llegar como promedio a una dieta de consumo de 36,8 kilocalorías por kg de peso ideal por día, que significa el 96 % de las cifras de recomendación energética para este tipo de paciente.5,6
Los resultados de la dieta en días de diálisis y no diálisis
se reflejan en las tablas 1 y 2. Durante las 12 semanas del estudio se logró
aumentar el ingreso energético en el 16 % los días de diálisis,
su vez los carbohidratos, y los lípidos aumentaron en el 14,4 % y 20
% en días de no diálisis y de diálisis respectivamente.
Estos incrementos pueden evitar que el organismo utilice las
proteínas como reserva energética, la producción excesiva
de hidrogeniones, la probabilidad aumentada de acidosis metabólica y
el empeoramiento de la fase catabólica a expensas de una degradación
no deseada de aminoácidos por la vía neoglucogénica.12
Los valores de consumo de sodio disminuyeron en el 22,3 % los días de diálisis, hasta obtenerse un cumplimiento de la recomendación aceptable. Este resultado contribuye a la normalización de los niveles de sodio en sangre que se mantuvieron dentro de los límites permisibles. Estos cambios favorables, previenen el edema, la hipertensión y el edema pulmonar como complicaciones no deseadas.
Los niveles de potasio en la dieta aumentaron en el período de intervención por el aumento de las proteínas pero no de forma significativa para la salud, pues se mantiene en intervalo aceptable para la cifra de recomendación. Estos resultados se cumplen tanto en días de diálisis como no diálisis. Por esta razón se notó un comportamiento estable y favorable de potasio en sangre sin cambios significativos, con un ligero aumento de los valores al final del estudio. En cuanto al calcio, folatos y el hierro, se logró suplementar las necesidades del organismo con las dietas propuestas.
Con las dietas ofertadas se logró cumplir la recomendación, con
un incremento aceptable del 17,6 % de magnesio en los
días de diálisis. De igual forma, el fósforo aumentó
solamente el 4,5 % los días de diálisis.
En cuanto a la ingesta de líquidos, se puede decir que el nivel de adecuación
estuvo por debajo del límite esperado de
restricción: en relación con la medición de la vena cava
13 . Los pacientes permanecieron normohidratados
durante el período de intervención dietética, los valores
de la vena cava cambiaron según la ganancia, pérdida o no variación
de peso de los pacientes en estudio, sin cambios significativos. El 37,5 % de
la población aumentó su valor de la vena cava, el 37,5 % disminuyó
y la población restante (25 %) mantuvo un valor constante. Al realizar
la prueba t de Student para muestras independientes, no se obtuvieron cambios
significativos. La correlación del diámetro vena cava y el índice
de masa corporal fue de –0,35 y – 0,36 al inicio y al final del período
de la investigación, resultando no significativo.
Como se muestra en las tablas 1 y 2, se logra el aumento deseado en la ingestión dietética de los aminoácidos histidina, leucina, isoleucina y metionina, tanto en los días de diálisis como de no diálisis, comparado con el pilotaje, resultado de nuestro estudio que puede considerarse favorable, ya que algunos autores 14,15 (Kopple 1976, 2001) y (Furst 1989, 1997)14 habían planteado que la histidina mejora la retención de nitrógeno en el balance metabólico en el organismo del paciente renal y que a su vez, interviene en la síntesis de hemoglobina que es una proteína con vida media de 90 días, lo que coincide con el período de observación.
TABLA 1. Resultados obtenidos en la evaluación de
dietas. Días de diálisis. Pacientes con Insuficiencia Renal durante
Dieta de Intervención. CIMEQ-IFAL: 2002.
|
Diálisis
|
|||||
|
Pilotaje
|
Intervención
|
||||
|
Nutrientes
|
Promedio
|
Adecuación
|
Promedio
|
Adecuación
|
Diferencia
|
|
Kcal/kg/día*
|
30,6
|
30,5
|
36,8
|
96,5
|
16,0
|
|
gprot/kg/día**
|
1,0
|
83,3
|
1,4
|
116,0
|
32,7
|
|
Hc (g/día)*
|
241,3
|
80,4
|
284,6
|
94,9
|
14,4
|
|
Lip (g/día)*
|
61,4
|
68,2
|
79,4
|
88,2
|
20,0
|
|
Na (mg/día)*
|
2771,0
|
119,2
|
2254,6
|
96,9
|
22,3
|
|
K (mg/día)*
|
1676,3
|
89,4
|
1810,6
|
96,6
|
7,2
|
|
P (mg/día)*
|
1031,2
|
103,1
|
1076,7
|
107,7
|
4,5
|
|
Mg (mg/día)*
|
172,4
|
86,2
|
207,7
|
103,8
|
17,6
|
|
Líquidos (ml/día)*
|
696,8
|
99,5
|
776,0
|
110,9
|
11,3
|
|
Ca (mg/día)*
|
2123,3
|
151,7
|
2088,9
|
149,2
|
2,7
|
|
Folatos (mg/día)*
|
1,1
|
137,5
|
1,2
|
150,0
|
12,5
|
|
Fe (mg/día)*
|
37,3
|
37,3
|
46,0
|
46,0
|
8,7
|
|
Hist (g/día)***
|
1,8
|
61,0
|
2,3
|
76,1
|
15,1
|
|
Isoleuc (g/día)****
|
2,7
|
76,1
|
3,2
|
90.0
|
13,9
|
|
Leuc (g/día)***
|
4,6
|
64,3
|
5,6
|
77,8
|
13,4
|
|
Met (g/día)***
|
2,2
|
98,2
|
3,0
|
135,6
|
37,4
|
TABLA 2. Resultados obtenidos en la evaluación de dietas. Días de no diálisis. Pacientes con Insuficiencia Renal durante Dieta de Intervención. CIMEQ-IFAL: 2002.
|
Pilotaje
|
Intervención
|
||
|
Nutrientes
|
Promedio
|
Promedio
|
Diferencia
|
|
Kcal/kg/día*
|
2,2
|
23,8
|
1,5
|
|
gprot/kg/día**
|
0,3
|
0,96
|
0,16
|
|
Hc (g/día)*
|
169,01
|
202,39
|
33,38
|
|
Lip (g/día)*
|
61,58
|
56,27
|
5,71
|
|
Na (mg/día)*
|
1492,3
|
1491,8
|
0,5
|
|
K (mg/día)*
|
1333,1
|
1379,32
|
41,22
|
|
P (mg/día)*
|
669,56
|
796,12
|
126,57
|
|
Mg (mg/día)*
|
134,2
|
145,67
|
11,47
|
|
Líquidos (ml/día)*
|
595,67
|
651,72
|
56,05
|
|
Ca (mg/día)*
|
1939,71
|
2008.75
|
69,04
|
|
Folatos (mg/día)*
|
1,68
|
1,15
|
0,53
|
|
Fe (mg/día)*
|
33,02
|
34,6
|
1,58
|
|
Hist (g/día)***
|
0,95
|
1,4
|
0,45
|
|
Isoleuc (g/día)****
|
1,59
|
2,9
|
1,31
|
|
Leuc (g/día)***
|
2,7
|
3,48
|
0,78
|
|
Met (g/día)***
|
1,68
|
1,65
|
0,03
|
El aumento del 32,7 % en el consumo de proteínas los días de
diálisis, que se produce secundariamente a la liberación
dietética que significa la acción detoxificadora del tiempo expuesto
a la diálisis y los alimentos brindados durante este período de
tratamiento, conduce a su vez riesgos de ajustes para el metabolismo y el equilibrio
ácido-base que deben ser previstos, ya que en el organismo se liberan
iones H + , causando una depleción del bicarbonato en sangre con cambios
altamente significativos (p <0,001).
Por tanto, la reserva alcalina puede sufrir cambios desfavorables, lo que puede
ser causa de acidosis metabólica, si no se
tiene en cuenta la necesaria compensación durante el tratamiento con
las debidas dosis de bicarbonato y de diálisis.17
(Fig.1).
Fig.1. Comportamiento del bicarbonato en sangre.
Se observó una ligera disminución de urea en sangre en el 75
% de la muestra, resultado que puede deberse, a que en la
posible acidosis metabólica causada por la disminución del bicarbonato,
el anabolismo de la urea disminuya lentamente en el orden de salvar el bicarbonato
para neutralizar el exceso de H + en sangre y de esta forma compensar la acidosis.18
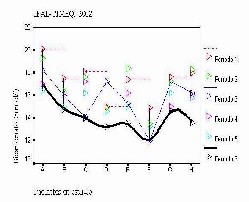
El aumento de proteínas en la dieta, además, influye en la síntesis de albúmina hepática en su efecto anabólico. En nuestro estudio se observó un incremento de dicha proteína en el 100 % de la muestra con cambios significativos (p <0,05) (Fig.2), lo que corrobora lo planteado por Davidson en 1979 3.
Fig.2. Variación de la albúmina y la hemoglobina
durante el estudio.
Como se puede apreciar en la figura 2, al final de la investigación existe un aumento de los niveles de hemoglobina en sangre en el 100 % de la muestra con diferencias significativas (p <0,05), resultado que puede confirmar lo planteado por Kopple (1976), y (Swendseid, 1981).9,14 Debe resaltarse, además, que este incremento estuvo condicionado por el suministro de eritropoyetina y de hierro oral. Los resultados demostraron una asociación significativa entre la hemoglobina y la albúmina sérica con los ingresos de nitrógeno y sus cambios en los días de diálisis durante las 12 semanas (p < 0,05), según prueba t de Student para muestras independientes.
Por otra parte, el consumo aumentado de la histidina, al mejorar la retención
de nitrógeno, provoca una disminución secundaria de producción
de la creatinina, por ser este un metabolito final de la catabolia, resultado
que pudo demostrarse en el 75 % de los hombres estudiados. El consumo dietético
de isoleucina y leucina y su aumento con respecto al pilotaje, pudiera considerarse
un resultado favorable, ya que estos aminoácidos al ser ramificados tienen
un efecto protector sobre la confluencia de vías metabólicas y
su degradación que preceden al ciclo de transformaciones del ácido
cítrico, de la compensación lograda con el aumento del ingreso
de estos aminoácidos ramificados, que tienen según Furst
un “patrón
especifico de catabolismo propio del enfermo renal” y que por ende tienen
una demanda aumentada en su metabolismo,
cuando estas demandas son compensadas se puede lograr mejorar la retención
de nitrógeno.14
De igual forma puede interpretarse que el incremento obtenido para la metionina, que es el agente metilante activo de la síntesis de compuestos como la epinefrina, acetilcolina y creatina, que son neurotransmisores y metabolitos del nitrógeno respectivamente. Durante los días de diálisis se logró alcanzar la composición de aminoácidos por masa corporal, sugerida por Swendseid, Kopple y colaboradores.9,14,15
En los días de no diálisis, en que la disponibilidad de alimentos del hogar y la colaboración de los pacientes no fue siempre satisfactoria. Los consumos dietéticos de histidina y metionina en mg/g de proteína consumida estuvieron bajos en relación con las referencias empleadas para pacientes renales durante los días de diálisis. Los resultados se pueden observar en la tabla 4.
TABLA 3. Comparación del contenido aminoacídico (mg aminoácidos/Kg de peso). Pacientes con Insuficiencia Renal durante Dieta de Intervención. CIMEQ-IFAL: 2002. * Recomendaciones para personas sanas (19) ** Referencia de Nefrosteril (8)
|
Aminoácidos
|
||||
|
(mg/Kg peso)
|
Diálisis
|
No diálisis
|
Sano*
|
Referencia*
|
|
Histidina
|
34,21
|
14,53
|
12,0
|
44,92
|
|
Isoleucina
|
47,79
|
23,95
|
10
|
53,3
|
|
Leucina
|
83,8
|
83,8
|
14
|
107,6
|
|
Metisonina
|
45,16
|
45,16
|
13
|
33,13
|
TABLA 4. Comparación del contenido aminoacídico (mg de aminoácidos/g proteína). Pacientes con Insuficiencia Renal durante Dieta de Intervención. CIMEQ-IFAL:2002. *Recomendaciones para personas sanas (7)
|
Aminoácidos (mg/g Proteina)
|
Diálisis
|
No diálisis
|
Sanos*
|
|
Histidina
|
37,72
|
21,8
|
11
|
|
Isoleucina
|
43,7
|
39,66
|
13
|
|
Leucina
|
64,8
|
54,25
|
19
|
|
Metisonina
|
43,9
|
28,48
|
17
|
En la ingestión dietética durante los días de diálisis se logran incrementos satisfactorios para los 4 aminoácidos previstos, de los cuales se destacan la isoleucina y la leucina. En el caso de este último, hubo un aumento de hasta 7 veces del aminoácido con respecto a la referencia de un sujeto sano, según se expresa en el comité de expertos para proteínas de 1985;7 pero cuando se le relaciona con cifras estimadas para un paciente renal estos incrementos estuvieron en el 70 % de la cifra deseada.
La isoleucina tuvo cifras de ingestión con 3 veces de incremento, con
respecto a la referencia del hombre sano, mientras que
alcanza el 90 % de la estimación realizada a partir de la composición
del Nefrosteril.
En los resultados de las pruebas antropométricas se observaron variaciones
aceptables en cuanto al peso, donde del total de pacientes en estudio, sólo
2 casos estuvieron fuera de los limites de normalidad para el índice
de masa corporal: uno en franca obesidad (caso B), y otro en el limite de la
desnutrición ligera (caso G). Este resultado es favorable, ya que se
logró alcanzar el peso ideal deseado en el 66,6 % de los hombres de la
investigación durante las 12 semanas de estudio. El 33,4 % de los pacientes
continuó por encima de su peso ideal al final de las observaciones y
solamente el caso del paciente desnutrido mantuvo el mismo valor de la evaluación
inicial. Esto coincide con los datos del informe dietético sobre el ingreso
energético
corroborando que se haya logrado un estado de equilibrio energético durante
la intervención dietética para los días de diálisis
(36,8 cal/Kg/día) y no diálisis (23,8 cal/Kg/día) (tablas
1, 2 y 5).
TABLA 5. Resultados de las mediciones antropométricas. Pacientes con Insuficiencia Renal durante la dieta de Intervención. CIMEQ-IFAL:2002.
|
Estatus
|
Peso ideal
|
Pesp (inicial)
|
Peso (final)
|
ICM (inicial)
|
IMC (final)
|
||
|
Pacientes
|
Edad
|
(cm)
|
(Kg)
|
(Kg)
|
(Kg)
|
(Kg/m2)
|
(Kg/m2)
|
|
A
|
44
|
175
|
75
|
61
|
60
|
19,9
|
19,6
|
|
B
|
45
|
156
|
56
|
86
|
84
|
35,4
|
34,6
|
|
C
|
52
|
178
|
28
|
86
|
82,4
|
27,1
|
26
|
|
D
|
54
|
157
|
57
|
59
|
50
|
23,9
|
23,9
|
|
E
|
39
|
166
|
66
|
70
|
71
|
25,5
|
25,8
|
|
F
|
47
|
162
|
52
|
55
|
56
|
20,9
|
21,39
|
|
G
|
37
|
163
|
63
|
47
|
47
|
17,5
|
17,7
|
|
H
|
45
|
175
|
75
|
73
|
76
|
23,8
|
24,84
|
|
Promedio
|
45,38
|
166,50
|
66,50
|
67,13
|
66,93
|
24,28
|
24,29
|
Durante los 90 días de intervención dietética no se observó incidencia de complicaciones en los pacientes del estudio.
Debe destacarse que en nuestra investigación, el uso de un patrón de dieta con alimentos comunes, económicos, de fácil adquisición en el mercado y de sencilla elaboración (figuras 3 y 4), fueron capaces de sustituir, en cuanto a la composición aminoacídica,19-20 las necesidades del patrón de catabolismo de este tipo de paciente, sustituyendo aquellos suplementos farmacéuticos, que son de alto costo y en determinadas ocasiones de difícil acceso para la población.
Fig.3. Distribución aminoacídica de los alimentos energéticos.
Fig.4. Distribución aminoacídica de los alimentos constructores.
El soporte nutricional sobre los pacientes con insuficiencia renal crónica
en hemodiálisis, constituye un elemento primordial e indispensable, tanto
para mejorar la calidad de vida, como para disminuir la frecuencia de complicaciones,
favoreciendo la
disminución de la morbilidad y la mortalidad.
De acuerdo con los resultados de este trabajo con una dieta que se apoya en
alimentos naturales y de fácil adquisición,
se aprecian cambios favorables de la síntesis de algunos marcadores,
lo que coincide con los planteamientos postulados por algunos autores.
A prospective investigation of the nutritional and metabolic balances of 8
male patients with End-Stage Renal Disease (ESRD) during dialytic treatment
was performed. The patients were exposed during 12 weeks to a dietetic intervention
consisting of: 1) recording the consumption of foods and 2) a menu tailored
to meet the needs of the patient during the 3 days of dialysis. The diet was
planned according with the criteria set forth by both the XV Food Guidelines
of the American Association of Nephrology and the FAO/WHO Experts Committee
on Proteins. The following variables were measured: serum Albumin, Haemoglobin,
Bicarbonate, Ionogram, Creatinine, Urea, Uric acid. The Body Mass Index (BMI)
was also calculated, and the diameter of the cava vein was estimated by ultrasonographic
means. Data proccessing was performed taking into account the
normality of the measured variables, their distributions and means. t-Student
test was applied in the case of independent
variables, along with stepwise regression analysis for selected variables. Results.
The results showed a significant association between Haemoglobin and Albumin
on one hand, and nitrogen intake and their changes in the days of dialysis during
the intervention period (p < 0.05, t-Student test for independent variables).
No patient showed any complication during the period of the study. Intakes of
nitrogen, histidine, leucine, isoleucine and methionine were controlled. Conclusions.
It is concluded the importance of the use of the diets made from natural foods
for the nutritional support of the ESRD patient with an specific catabolic pattern
in view of their low cost, feasibility, and capability to increase the metabolic
efficiency of the patient.
Subject headings: Haemodialysis / Aminoacids / Metabolic Efficiency / Catabolism Pattern / Tailored designed Diets.
1 Licenciada en Alimentos. Departamento de Alimentación.
Centro de Investigaciones Médico-Quirúrgicas (CIMEQ).
2 Doctora en Ciencias Médicas. Especialista de II Grado
en Nutrición y Metabolismo. Investigadora Titular.
Centro de Investigaciones Médico-Quirúrgicas (CIMEQ).
3 Especialista de I Grado de Nefrología. Centro de Investigaciones Médico-Quirúrgicas (CIMEQ).