ACTA MEDICA 1998;8(1):86-100
Medicamentos antivirales
Dr. JESÚS BARRETO PENIÉ,1 Dr.
JOSÉ GUNDIÁN GONZÁLEZ-PIÑERA,2 Dr.
MIGUEL A. RODRÍGUEZ RODRÍGUEZ,3 Dr. PEDRO P.PINO
ALFONSO4
RESUMEN
Se revisan los mecanismos y sitios de acción de los diferentes
agentes y drogas contra los virus más frecuentes que producen enfermedades
de importancia clínica y epidemiológica. El desarrollo de
la biología molecular y las tecnologías de avanzada han permitido
conocer las distintas etapas de la multiplicación de los ácidos
nucleicos y proteínas de los virus; estos pasos pueden constituir
puntos críticos o blancos donde actúen sustancias químicas
de origen natural o diseñadas especialmente mediante técnicas
sofisticadas que entorpecen, e incluso detienen la duplicación viral.
El objetivo principal es acercar al médico de asistencia a este
tema de poca aplicación práctica en nuestro entorno clínico.
La terapia antiviral ha entrado en una época de progreso que va
desde la impotencia terapéutica a la posibilidad actual de tratar
muchas enfermedades virales. No estarán lejos los días en
que los médicos necesitarán conocer tanto sobre el tratamiento
de las infecciones virales como sobre sus similares bacterianas.
Descriptores DeCS: AGENTES ANTIVIRALES/farmacocinética.
INTRODUCCIÓN
Los avances en la quimioterapia de las enfermedades virales son mucho menores
que los alcanzados en el tratamiento de las infecciones bacterianas. En
Estados Unidos están disponibles sólo unos pocos agentes
antivirales de valor clínico demostrado. Un análisis de los
problemas asociados al desarrollo de estos medicamentos muestra que:
-
Los virus son parásitos intracelulares obligados que utilizan muchas
vías bioquímicas y metabólicas de las células
hospederas infectadas.
-
Ha resultado difícil alcanzar una actividad antiviral útil
sin afectar el metabolismo normal de la célula infectada, causando
también efectos tóxicos en células no infectadas.
-
El diagnóstico temprano de la infección viral es crucial
para garantizar una terapia antiviral efectiva, debido a que una vez que
los síntomas aparecen, numerosos ciclos de multiplicación
viral ya han ocurrido y la duplicación comienza a disminuir. Por
esto, un tratamiento efectivo depende de medios diagnósticos rápidos,
sensibles, específicos y prácticos.
-
Como la mayoría de las enfermedades virales son bastante comunes,
relativamente benignas y autolimitadas; el índice terapéutico
(relación eficacia/toxicidad) debe ser elevado para que un tratamiento
sea aceptable.
La explosión actual de investigaciones en biología molecular
está ayudando a solucionar algunos de esos problemas. Ha sido posible
identificar enzimas únicas en la duplicación viral y de esta
manera distinguir claramente entre funciones del virus y la célula
hospedera. Acontecimientos únicos en la multiplicación viral
constituyen sitios que sirven como blancos ideales para las drogas antivirales.
Como ejemplos se mencionan la timidina-quinasa del virus herpes simple
y la transcriptasa reversa del virus de inmunodeficiencia humana (HIV).11
Por otro lado, el desarrollo de métodos diagnósticos sensibles
y específicos ha sido posible por la tecnología del DNA recombinante,
el uso de anticuerpos monoclonales, técnicas de hibridación
de DNA y recientemente el uso de «la reacción en cadena de
la polimerasa» que permite la detección de un genoma viral
en una muestra de tejido.2
La quimioterapia antiviral ha experimentado una revolución en
las 2 últimas décadas. Los éxitos en la búsqueda
de una terapia antiviral efectiva y práctica han tenido su origen
en avances de las ciencias químicas, biología molecular y
virología. Han sido descubiertos -o creados mediante técnicas
ingenieras- compuestos que son capaces de distinguir entre las funciones
de la célula hospedera, de las funciones virales específicas
con discriminación suficiente para ser efectivas en el tratamiento,
pues tienen elevada eficacia antiviral y toxicidad mínima para las
células infectadas.3
La disponibilidad de una quimioterapia antiviral efectiva igualmente
se nutre de mejoras en las técnicas de identificación de
los virus. El empleo apropiado de esta terapia también depende en
la actualidad de un diagnóstico rápido con medición
precisa de la carga viral (antígeno o ácido nucleico viral)
en el individuo infectado para monitorizar la respuesta al tratamiento.
MECANISMOS DE ACCIÓN
Los virus pueden ser divididos en 2 grandes grupos sobre la base de si
contienen DNA o RNA en sus ácidos nucleicos. El análisis
de estos ácidos nucleicos virales y las proteínas por ellos
codificadas han proporcionado a los científicos un sitio potencial
para blanco de las drogas antivirales. Muchas de las proteínas-!diana
son componentes no estructurales del virus. Ej. enzimas involucradas en
la multiplicación. Para comprender el mecanismo de acción
de las drogas, es necesario considerar el ciclo vital completo de un virus
típico, que puede ser desglosado en 5 pasos o etapas (fig. 1):
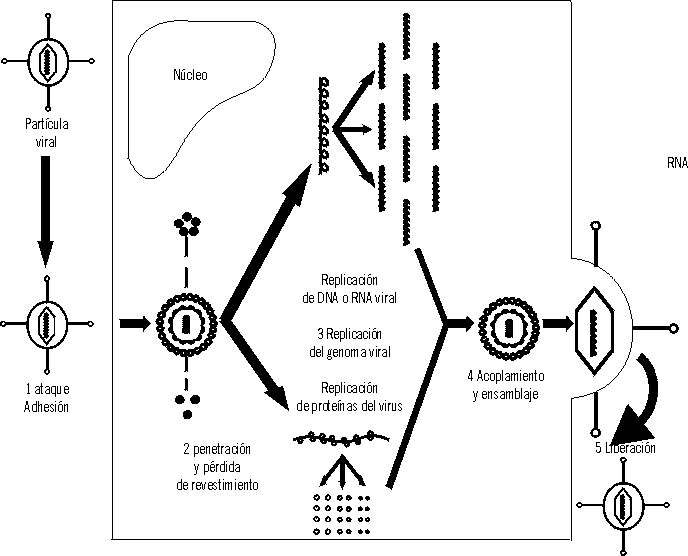 FIG. 1 Ciclo vital típico de un virus.
FIG. 1 Ciclo vital típico de un virus.
-
Adhesión.
-
Penetración.
Pérdida del revestimiento.
-
Duplicación del genoma viral.
Duplicación de las proteínas virales.
-
Ensamblaje o armadura.
-
Liberación.
PASO 1. ADHESIÓN A LA CÉLULA POR INTERACCIÓN CON UN
RECEPTOR ESPECÍFICO SITUADO EN LA MEMBRANA CELULAR
Los polisacáridos sulfatados como el sulfato de dextrán inhiben
el transporte del HIV a su receptor celular, la proteína CD4.4,5,6
Otro enfoque estratégico consiste en saturar esta proteína
con CD4 recombinante soluble, quien se une al virus y bloquea la adhesividad
del HIV (este efecto sólo ha sido logrado con efectividad en el
laboratorio).7
PASO 2. PENETRACIÓN Y PÉRDIDA DEL REVESTIMIENTO O ENVOLTURA
DEL VIRUS QUE RESULTA EN LA LIBERACIÓN Y ACTIVACIÓN DEL GENOMA
VIRAL
En general, este proceso no es bien conocido, aunque se requiere de funciones
celulares. La amantadina y su derivado rimantadina inhiben al virus de
la influenza A en este paso. Sus efectos antivirales se incrementan por
interacción con la proteína de matriz viral codificada M2;
ésta forma canales iónicos por donde los protones atraviesan
las membranas de vesículas endocíticas intracelulares.8
La amantadina bloquea esta transferencia de protones mediadas por M2 que
inhibe así la pérdida de revestimiento viral. Aunque estos
medicamentos no tienen amplia aceptación para su empleo profiláctico,
ofrecen una buena opción para la vacunación activa en la
epidemia por influenza A.1
Algunos compuestos actúan exclusivamente en la pérdida
del revestimiento, Ej. arildone, que inhibe selectivamente la multiplicación
de algunos enterovirus, rinovirus y herpesvirus in vitro. Una optimización
cuidadosa de la estructura/actividad ha llevado a la aparición de
derivados más activos y de amplio espectro (WIN 51711) que inhiben
numerosos serotipos de rinovirus y enterovirus.9 Sin embargo,
sus reacciones adversas son a menudo suficientes para eliminar estas drogas
como terapias potenciales.
PASO 3. DUPLICACIÓN DEL GENOMA VIRAL Y PRODUCCIÓN DE PROTEÍNAS
VIRUS-ESPECÍFICAS (ESTRUCTURALES Y NO ESTRUCTURALES)
La mayoría de las drogas antivirales efectivas que actúan
en este nivel son análogos de los nucleósidos requeridos
para la síntesis de nuevos DNA y RNA virales. La síntesis
de ácidos nucleicos virales es guiada por una enzima codificada
por el virus, tanto cuando el ácido nucleico creciente está
siendo extendido por la adición de nucleótidos, como durante
la fosforilación de estos últimos.10 Ejemplos
de enzimas virus-específicos participantes en la duplicación
del genoma son la timidina-quinasa del virus herpes simple, la DNA polimerasa
DNA-dependiente del citomegalovirus y herpes simple y la transcriptasa
reversa viral (DNA polimerasas RNA-dependiente) del HIV y el virus de la
hepatitis B. La activación de esos análogos de glucósidos
es tanto selectiva (guiadas por el virus), Ej. aciclovir, como no selectiva
(guiada por la célula hospedera), Ej. zidovudina.
Aciclovir. El arte y ciencia de la síntesis de análogos
de nucleósidos ha florecido durante décadas en la búsqueda
ocasionalmente exitosa de drogas contra el cáncer. El aciclovir
es un análogo de guanosina acíclico (el componente glucídico
ribosa no cierra el anillo y pierde el sitio 3-hidroxilo, donde la elongación
de la cadena de DNA ocurre normalmente). En su forma trifosfatada, el medicamento
inhibe la DNA polimerasa y la replicación del DNA viral, y causa
una terminación prematura de la cadena de DNA viral.11,12
La fosforilación y activación de la droga ocurre en 3 etapas
(fig. 2). Está ligada directamente a la presencia de la timidina-quinasa
del virus del herpes simple. Enzimas celulares convierten el monofosfato
de aciclovir generado por el virus, en trifosfato de aciclovir con actividad
antiviral. Esta fosforilación selectiva del aciclovir por la timidina-quinasa
asegura un índice elevado de actividad antiviral y efectos adversos
mínimos.13
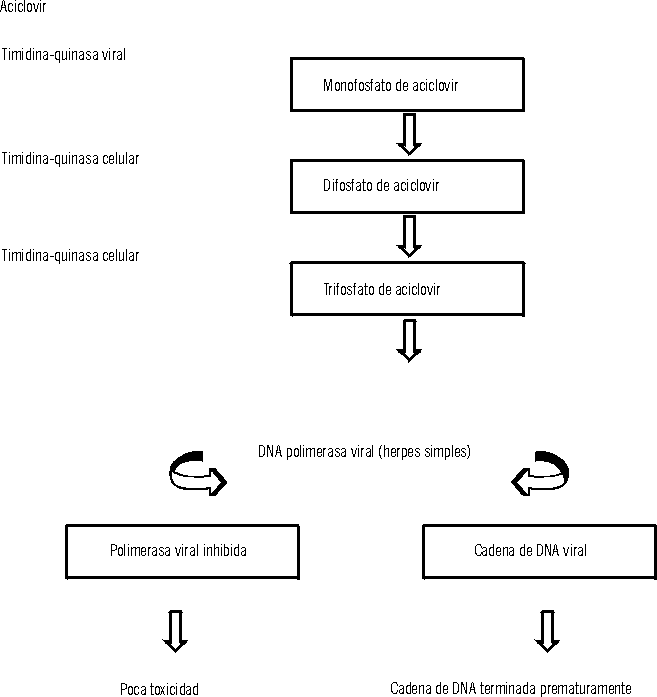 FIG. 2 Metabolismo del aciclovir en células infectadas por
virus.
FIG. 2 Metabolismo del aciclovir en células infectadas por
virus.
Zidovudina. Es un análogo nucleósido no selectivo empleado
para la infección por HIV. Al igual que el aciclovir, debe ser fosforilado
para su actividad; sin embargo, no involucra enzimas virales, sino sólo
de la célula hospedera. El trifosfato de zidovudina inhibe la transcriptasa
reversa del HIV, así como el crecimiento de la cadena del DNA viral
(fig.3). Debido a que la zidovudina es activada por enzimas de las células
hospederas, produce también efectos indeseados en las células
no infectadas, por lo que su empleo se asocia con efectos adversos incluyendo
la anemia.14
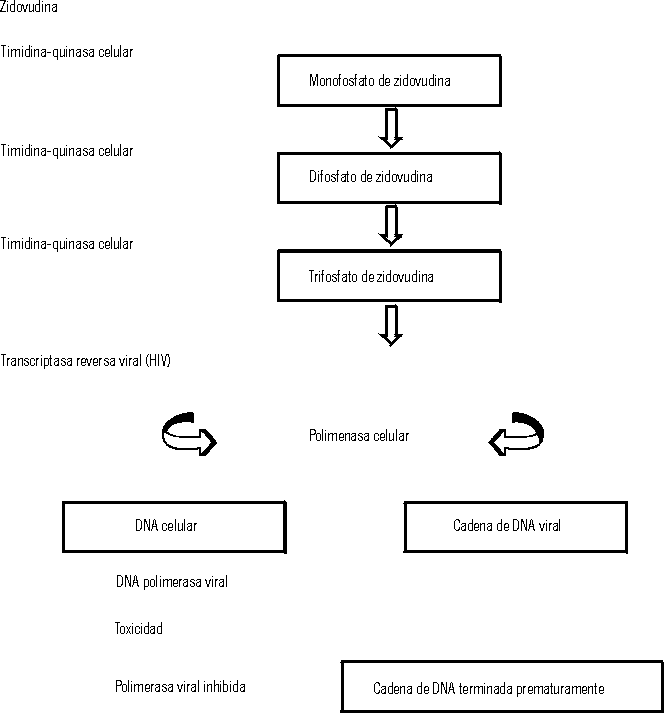 FIG. 3 Metabolismo de la zidovudina en células infectadas
por virus.
FIG. 3 Metabolismo de la zidovudina en células infectadas
por virus.
Otros análogos de nucleósidos no selectivos son dideoxicitidina
(ddC/zalcitabina), dideoxiinosina (ddI/didanosina), y ganciclovir. Tanto
el ddC como el ddI son inhibidores potentes de la transcriptasa reversa
del HIV y, en la actualidad, constituyen los agentes antivirales de segunda
línea en el tratamiento de la infección por HIV.15-17
Ganciclovir. Es un análogo nucleósido acíclico
de la guanosina y es similar en estructura al aciclovir.18 Es
activa contra todos los herpes virus humanos y es una de las pocas drogas
antivirales que tienen actividad in vivo contra los citomegalovirus.19
También es más tóxica que el aciclovir y por esta
razón es usada principalmente en el tratamiento de las infecciones
severas por CMV en pacientes inmunocomprometidos, y en la infección
grave por el virus de la hepatitis B.20
En resumen, los análogos de nucleósidos selectivos y no
selectivos poseen un doble modo de acción:
-
Inhiben la duplicación del DNA viral mediante la terminación
prematura de la cadena de DNA en formación.
-
En su forma trifosfatada, compiten con las bases nucleótidas naturales
por las polimerasas virales.
Existen otros sitios en las polimerasas que pueden ser blancos de las drogas
antivirales. Uno de tales regiones es el sitio de transporte de pirofosfatos
donde ocurre un intercambio de esta sustancia durante la duplicación
del DNA. El foscarnet (fosfonoformato) es un inhibidor potente de este
proceso.21 Aunque la polimerasa viral es más sensible
al foscarnet, la polimerasa celular también puede afectarse, y ocasionar
mayor toxicidad (disfunción renal).19 La droga es usada
en ocasiones para tratar infecciones muy graves por virus del herpes simple
y hepatitis B y D. También tiene un papel relevante en el tratamiento
de las infecciones por virus herpes simple resistentes al aciclovir, así
como infecciones por CMV refractarias a la terapia con ganciclovir.21
SÍNTESIS DE PROTEÍNAS VIRALES
La síntesis de proteínas virales ocurre en el citoplasma
de las células infectadas. Los ribosomas de las células hospederas
son usados para producir proteínas estructurales (núcleo
y cubierta o envoltura), y no estructurales (polimerasas DNA/RNA, timidinaquinasa).
Este paso es el blanco de acción de los interferones. Los interferones
(IFN) son una familia de glucoproteínas producidas por el huésped,
como parte de su defensa natural contra las infecciones.22 Son
citoquinas con propiedades complejas de tipo inmunomoduladores, antineoplásicas
y antivirales. Se clasifican en a, ß ó g (sus fuentes naturales
son los leucocitos, fibroblastos y linfocitos respectivamente).23
Cada tipo de IFN hoy día puede obtenerse por la técnica del
DNA recombinante. Ellos inhiben los virus de forma indirecta, primero por
unión a receptores celulares y luego, al inducir la producción
de enzimas intercelulares. Esto interrumpe la multiplicación viral
por el bloqueo total de la síntesis de proteínas y el recambio
de RNA. Los interferones también exhiben funciones inmunorreguladoras,
incluyendo la activación de la inmunidad mediada por células,
especialmente las células asesinas naturales, linfocitos T citotóxicos
y macrófagos.24
La ribavirina es un análogo de nucleósido que estructural
y funcionalmente se asemeja a la guanosina. Es activa contra una amplia
gama de virus DNA y RNA in vitro, pero tiene pobre actividad in
vivo. Numerosos mecanismos de acción han sido propuestos; en
su forma monofosfatada, la ribavirina es un inhibidor competitivo potente
de la enzima dehidrogenasa quien es esencial para la síntesis de
trifosfato de guanosina.25 Esta inhibición resulta en
una disminución en los depósitos celulares de guanidina,
necesaria tanto para la multiplicación viral como celular. Sin embargo,
su mayor efecto antiviral de significación es la inhibición
en la terminación o punto final del RNA mensajero viral y produce
una caída en la producción de proteínas virales.26
También ha sido autorizado su empleo en niños con bronquiolitis
severa debidas al virus sincitial respiratorio.15-27
PASOS 4 Y 5. MONTAJE Y ACOPLAMIENTO DE LOS COMPONENTES VIRALES DENTRO DE
UN VIRUS DESCENDIENTE Y LIBERACIÓN DE PARTÍCULAS VIRALES
COMPLETAS DENTRO DEL ENTORNO EXTRACELULAR
Las últimas 2 etapas del ciclo vital de multiplicación viral
son comprendidas de manera incompleta. Los depósitos de los genomas
recientemente copiados (RNA y DNA) interactúan con los depósitos
de los elementos estructurales nucleares de síntesis reciente y
producen nucleocápsides del virus hijo, quien madura después
por germinación, usualmente a través de la membrana celular
obtiene la envoltura viral. Los interferones también bloquean en
este paso la duplicación viral.1,14,24
Las proteasas codificadas virales actualmente representan un nuevo objetivo
de la quimioterapia antiviral, Ej. la proteasa del HIV, que es reponsable
del procesamiento de una poliproteína precursora viral dentro de
los componentes estructural y no estructural. Esto permite un acoplamiento
y maduración de viriones infectivos de HIV. Un número de
inhibidores selectivos de la proteasa del HIV han sido identificados y
son evaluados en ensayos clínicos de fase I. La tabla 1 resume las
drogas y los mecanismos del ciclo vital del virus.
TABLA 1. Avances en el desarrollo de agentes quimioterapéuticos
activos contra los virus
| Ciclo vital del virus |
|
| Pasos o etapas |
Drogas
|
| 1. Ataque o adhesión |
. Polisacáridos sulfatados (sulfato de
dextrán) |
| |
. CD4 recombinante soluble |
| 1. Penetración |
. Amantadina/rimantadina (solamente para virus
de influenza A) |
| Pérdida del revestimiento |
. Arildone y WIN 51711 (rinovirus y enterovirus) |
| 2. Duplicación del genoma viral |
Inhibidor selectivo |
| |
. aciclovir (herpes simple y zóster) |
| |
Inhibidor no selectivo |
| |
. AZT, ddC, ddI (HIV) |
| |
. Foscarnet (CMV y hepatitis B y C) |
| |
. Ganciclovir (CMV) |
| Duplicación de proteínas del virus |
. Interferones (hepatitis B, C y D) |
| |
. Ribavirina (virus sincitial respiratorio) |
| 4. Ensamblaje y acoplamiento |
. Interferones (HIV) |
| |
. Interferones (HBV) |
| |
. Inhibidores de proteasas (HIV) |
| 5. Liberación |
. Interferones (HIV) |
QUIMIOTERAPIA COMBINADA
Existen muchos procesos claves en el ciclo vital viral que son susceptibles
para la intervención de las drogas antivirales. El empleo de combinaciones
de esas drogas al actuar en diferentes pasos del ciclo de multiplicación,
pueden resultar en una inhibición sinérgica significativa
del virus con reducción de su toxicidad celular y resistencia a
las drogas. Combinaciones de análogos de nucleósidos (como
aciclovir y zidovudina) o un análogo de nucleósido con un
interferón están resultando alternativas muy útiles
a la monoterapia.
DIRECCIONES FUTURAS
Estos avances pueden traer como resultado una mayor aplicación de
las drogas existentes, tanto en enfermedades diferentes como en estados
patológicos, en la elección de combinaciones sinérgicas
más potentes o en la combinación con drogas que reducen toxicidad.
Un buen ejemplo de esta última posibilidad está en el uso
de varios factores de crecimiento hematológico (como el GM-CSF o
G-CSF) para disminuir la toxicidad en la médula ósea de análogos
de nucleósidos como el ganciclovir.5
La próxima década será testigo del dramático
progreso en el desarrollo de las drogas antivirales. El advenimiento de
nuevas técnicas de modelado matemático, la cristalografía
por Rx y la imagen por resonancia magnética jugarán papeles
significativos en la creación de nuevos agentes antivirales. El
diseño de drogas mediante técnicas computadorizadas aún
esta en sus albores y drogas no antivirales han sido obtenidas de nuevo
mediante esta técnica. No obstante, se avanza rápidamente
y existen promesas para la identificación selectiva y eficiente
de nuevas drogas.
EMPLEO CLÍNICO
La utilización de drogas antivirales se está convirtiendo
en algo cotidiano, tanto en el ámbito hospitalario como en el comunitario,
de modo que un número cada vez mayor de agentes antivirales serán
empleados en los próximos años. La terapia antiviral efectiva
es importante especialmente para los enfermos inmunocomprometidos, pero
el tratamiento de los menos afectados (infecciones virales comunes adquiridas
en la comunidad), es también un objetivo deseable.
El arsenal y dispendio de las drogas antivirales varía según
su uso. Unos pueden ser prescritos por médicos generales, otros
son restringidos a unidades especializadas de grandes hospitales, mientras
que otros están en fase de investigaciones y ensayos, por lo que
se requiere de licencias especiales para su empleo en algunos países.
Nos limitaremos al tratamiento de las infecciones víricas no retrovirus
(HIV), pues éstas siempre se tratan como tema independiente, dada
su complejidad.
ACICLOVIR
PROPIEDADES
Activo in vitro e in vivo contra los tipos 1 y 2 de herpes virus,
y el virus de la varicela-zóster, su toxicidad es baja para las
células infectadas del hombre y los mamíferos.
INDICACIONES
-
Herpes virus genital (infección primaria): el tratamiento oral es
suficiente en la mayoría, aunque la forma parenteral puede usarse
en infecciones graves o complicadas.
-
Herpes virus genital recurrente: definido por más de 6 ataques por
año; puede ser suprimido por aciclovir en tratamiento prolongado.
La droga no es efectiva para tratar recurrencias individuales.
-
Herpes virus oro-labial: debe ser reservado para pacientes inmunocomprometidos
o individuos inmunocompetentes con infecciones primarias graves.
-
Encefalitis por herpes virus: es el tratamiento de elección debido
a la considerable reducción de la morbilidad y la mortalidad de
esta enfermedad.
-
Herpes zóster: es efectivo en el tratamiento de esta entidad en
pacientes inmunocompetentes.
-
Otros usos: Profilaxis en pacientes con trasplante de médula ósea
con anticuerpos positivos para herpes virus en el período inmediato;
también puede reducir la intensidad de la enfermedad por citomegalovirus
en trasplantados (receptores de órganos sólidos).
Infecciones por virus de varicela-zóster. Las indicaciones están
cambiando, debido a las diferentes opiniones entre los expertos.27,28
-
Herpes zóster (zona). En el paciente inmunodeprimido debe ser tratado
para evitar su diseminación.
-
Herpes zóster oftálmico debido al riesgo de complicaciones
intraoculares.
-
Los ancianos tienen episodios más graves y el empleo temprano de
aciclovir (dentro de las 72 horas de su aparición), acelera la resolución
del rash y reduce el dolor agudo. Su uso fuera de este contexto
resulta inefectivo.
Varicela. Estudios recientes han demostrado que el tratamiento precoz (dentro
de las 24 horas del comienzo del rash) puede acortar la duración
de la enfermedad en niños, adolescentes y adultos.29,30
El desarrollo de resistencia por el uso amplio del medicamento es una discusión
teórica, no obstante, no se recomienda su uso en niños con
varicelas, pero sí en adultos donde la enfermedad es más
grave con complicaciones frecuentes.
POSOLOGÍA
Adultos con función renal normal
Infecciones por herpes virus simple tipo I: un comprimido (200 mg)
5 veces al día, cada 4 horas omitiendo la dosis nocturna durante
5 días. En pacientes inmunodeprimidos 400 mg 5 veces al día.
Para la supresión de las recurrencias en pacientes inmunocompetentes:
200 mg 4 veces al día cada 6 horas o 400 mg cada 12 horas. Interrumpir
el tratamiento cada 6-12 meses para observar evolución.
Profilaxis en pacientes inmunocomprometidos: 200 mg 4 veces al
día. En pacientes con depresión inmunológica grave
la dosis se puede duplicar.
Infecciones por herpes zóster. En general requieren de
dosis mayores que en el herpes virus: 800 mg 5 veces al día es suficiente
para la mayoría de las infecciones en huéspedes inmunocomprometidos
incluyendo la fase oftálmica. La vía EV se calcula a 10 mg/kg
3 veces al día para inmunodeprimidos.
El tratamiento oral es adecuado para pacientes con zonas y bajo riesgo
de diseminación, así como en aquéllos con HIV o que
reciben dosis bajas de esteroides.
Otro esquema
800 mg cada 12 horas en pacientes con filtrado glomerular menor de 10 mL/min
y 800 mg cada 6 u 8 horas en pacientes con filtrado mayor de 10-25 mL/min.
En los ancianos se recomienda un aporte líquido adecuado mientras
se encuentren en tratamiento.
Niños
Los mayores de 2 años emplearán las dosis de los adultos.
Los menores de 2 años emplearán la mitad de la dosis de
los adultos.
El aciclovir parenteral se debe administrar por vía EV exclusiva.
Se emplea para las infecciones por herpes virus en pacientes inmunodeprimidos.
La dosis es de 5 mg/kg en infusión en 1 hora, que se repite cada
8 horas hasta una dosis total de 15 mg/kg/día durante 7 días.
Con este esquema se ha obtenido una mejora de las lesiones clínicas
en las primeras 48 horas, y una remisión total en 7 días.
Para las formas diseminadas o encefalitis se duplicará esta dosis
en el tiempo (14 días).
En Cuba se ha utilizado el aciclovir en el tratamiento de la encefalitis
herpética con esquemas de 10 mg/kg/día durante 7 días
con buenos resultados.31
Las lesiones mucocutáneas en pacientes inmunocomprometidos se
tratan a 250 mg/m2 de superficie corporal EV en infusión (1 hora)
cada 8 horas durante 7 días.
ACICLOVIR TÓPICO
Infecciones oculares. Indicado en pacientes con conjuntivitis y/o
queratitis por herpes simple. En pacientes con varicela-zóster oftálmico
tratados con aciclovir sistémico, el nivel de la droga en lágrimas
es probablemente suficiente para tratar cualquier queratitis o conjuntivitis
asociada. No obstante, la forma tópica (ungüento oftálmico)
también se recomienda.
La crema se aplica localmente en las lesiones cutáneo-mucosas
5 veces al día. Si no mejora, continuar 5 días más.
No aplicar en los ojos.
CONTRAINDICACIONES
-
Pacientes con hipersensibilidad conocida al aciclovir.
-
Embarazo.
-
Lactancia.
INTERACCIONES MEDICAMENTOSAS
La administración simultánea con provenecid aumenta la vida
media del aciclovir. Los medicamentos que alteran la función renal
podrían modificar la farmacocinética del aciclovir.
EFECTOS SECUNDARIOS
-
Pueden aparecer náuseas y cefalea con dosis orales elevadas (800
mg 4-5 veces/día). La vía EV puede causar deterioro de la
función renal, debido a su precipitación en los túbulos
renales en pacientes con enfermedad renal preexistente, especialmente en
el anciano.
-
Son raros los efectos adversos neurológicos (vértigos, confusión,
letargo, delirio), y ocurre por lo general cuando las dosis EV no se reducen
en pacientes con daño renal.
-
Los fabricantes no recomiendan su empleo durante el embarazo, aunque no
existen evidencias de daño fetal en la descendencia de un número
significativo de mujeres a quienes se les administró aciclovir durante
el embarazo.
-
Pueden elevarse las cifras de bilirrubina, enzimas hepáticas, azoados
plasmáticos. Su administración EV puede producir flebitis
en el sitio de inyección.
PRESENTACIÓN
Comprimidos de 400 mg
Comprimidos de 800 mg
Suspensión de 400 mg en 5 mL
Frascos de 100 mL
Frascos de 200 mL
Bulbos de 500 mg
Crema oftálmica al 5 %
GANCICLOVIR
INDICACIONES
-
Infecciones por citomegalovirus (CMV) que pongan en peligro la vida o afecten
gravemente la visión de pacientes inmunodeficientes (SIDA, trasplante
de órganos, quimioterapia anticancerosa.
-
Las infecciones antes mencionadas incluyen: retinitis, colitis, esofagitis,
gastroenteritis y neumonías.
-
En los pacientes con trasplantes de médula ósea se emplea
habitualmente en combinación con gamma-globulina CMV específica.
-
No se ha comprobado la eficacia y seguridad del medicamento en el tratamiento
de infecciones de menor gravedad.
-
Preventivo en pacientes receptores de órganos con riesgo elevado
de desarrollar la infección.
-
No está indicado en las infecciones congénitas o neonatales
por CMV, ni en sujetos inmunocompetentes.
-
Tiene un rol potencial en otras infecciones graves por CMV como la mononucleosis
en adultos inmunocomprometidos.
POSOLOGÍA
Tratamiento inicial
5 mg/kg EV en infusión en una hora cada 12 horas (10 mg/kg/día)
durante 2 ó 3 semanas.
Tratamiento de mantenimiento
El 50 por ciento de los pacientes tratados pueden hacer una recaída
en cuanto el medicamento es suspendido.32 Se emplea entonces
a 6 mg/kg/día durante 5 días a la semana; o 5 mg/kg/día
los 7 días de la semana si no se ha restaurado la función
inmune.
Tratamiento precoz-preventivo
Dosis de carga: 5 mg/kg cada 12 horas 1 ó 2 semanas.
Dosis de mantenimiento: 6 mg/kg/día 5 días a la semana;
5 mg/kg/día diariamente.
A los pacientes en régimen dialítico se recomienda 1,25
mg/kg/día justo después de la sesión.
El tratamiento con ganciclovir debe ser supervisado por una unidad especializada
y con experiencia en su empleo.
CONTRAINDICACIONES
-
Embarazo.
-
Lactancia.
-
Hipersensibilidad al fármaco o al aciclovir.
EFECTOS SECUNDARIOS
Durante los ensayos clínicos, el tratamiento con ganciclovir se
interrumpió en el 32 por ciento de los pacientes debido a la aparición
de efectos indeseables.33 Las manifestaciones más frecuentes
fueron: neutropenia (38 %), trombocitopenia (19 %), anemia, fiebre, rash
cutáneo (2 %). Otros efectos menos frecuentes:
-
Generales: escalofríos, edemas, malestar.
-
Cardiovasculares: arritmias, hipertensión, hipotensión.
-
Sistema nervioso: sueños delirantes, ataxia, confusión, mareos,
parestesias, nerviosismo, temblores.
-
Digestivos: náuseas, vómitos, anorexia, diarreas, cólicos.
-
Respiratorios: disnea.
-
Renales: hematuria, aumento de azoados.
-
Locales: flebitis, inflamación.
-
Laboratorio: alteraciones en la función hepática, disminución
de la glucemia.
-
Es potencialmente teratogénico y carcinogénico.
INTERACCIONES MEDICAMENTOSAS.
-
Su administración junto a la zidovudina puede producir neutropenia.
-
Tiene efectos tóxicos aditivos con: dapsona, pentamidina, fluorcitocina,
vincristina, trimetoprín, sulfamidas.
-
Su administración junto a imipenemcilastatina puede desencadenar
convulsiones generalizadas.
EMPLEO EN GRUPOS DE RIESGO
Embarazadas. Aunque no existen datos obtenidos en humanos, los estudios
en modelos animales recomiendan no administrar en este grupo de pacientes
debido a que existe un riesgo elevado de embriotoxicidad y fetotoxicidad.33
Lactancia. Se desconoce si la droga se excreta con la leche materna;
no obstante, por motivos de seguridad, no se debe administrar a la madre
que lacta. También por este motivo, la misma se restaurará
72 horas después de la última dosis de ganciclovir.
Niños. La experiencia clínica en niños menores
de 12 años es limitada, por lo tanto, se deberán extremar
las precauciones en casos pediátricos ante la posibilidad de aparición
de un efecto carcinógeno o alteraciones del aparato reproductor
a largo plazo.
En todos los casos se debe realizar un análisis exhaustivo y
considerar en primer término, la relación riesgos/beneficios.
PRESENTACIÓN
Ampolleta de 500 mg de ganciclovir como principio activo.
Cápsula de 250 mg.
FOSCARNET
Es un agente antivírico dotado de un amplio espectro de actividad,
de modo que inhibe a todos los virus humanos conocidos del grupo de herpes:
virus del herpes simple tipos 1 y 2, virus 6 del herpes humano, virus varicela-zóster,
virus de Ebstein-Barr y citomegalovirus.
INDICACIONES
-
Infecciones por citomegalovirus. Es tan efectivo como el ganciclovir para
el tratamiento de la retinitis por CMV en enfermos de SIDA. Se reserva
para pacientes con intolerancia a esta última droga. No se ha demostrado
la eficacia y la seguridad del foscarnet en el tratamiento de otras infecciones
por cito-megalovirus (neumonitis, gastroenteritis), ni en las formas congénitas
o neonatales del CMV en pacientes inmunocompetentes.
-
Infecciones por herpes virus y varicela-zóster. Enfermos inmunodeprimidos,
especialmente con SIDA o tratamiento supresivo con aciclovir por tiempo
prolongado, pueden desarrollar infecciones por herpes virus resistentes
al aciclovir. El foscarnet sería una opción efectiva para
estos casos, aunque puede desarrollarse también resistencia con
el tiempo. Asimismo ha sido empleado con éxito en infecciones por
el virus varicela-zóster rebeldes al aciclovir.34,35
POSOLOGÍA
Adultos
Tratamiento de inducción: en el paciente con función
renal normal, se puede administrar en forma de infusiones intermitentes
cada 8 horas a la dosis de 60 mg/kg (tabla 2). La dosis de foscarnet debe
ajustarse constantemente a la función renal (aclaramiento de creatinina).
La duración de cada infusión no debe ser inferior a una hora.
TABLA 2. Dosis de foscarnet
|
Tratamiento de inducción
|
Aclaramiento de creatinina
Mg/kg/min |
Infusión intermitente
Dosis: mg/kg
Cada 8 horas durante 1 hora |
|
> 1,6
|
60
|
|
1,6 - 1,4
|
55
|
|
1,4 - 1,2
|
49
|
|
1,2 - 1,0
|
42
|
|
1,0 - 0,8
|
35
|
|
0,8 - 0,6
|
28
|
|
0,6 - 0,4
|
21
|
|
< 0,4
|
Tratamiento no recomendado
|
|
Tratamiento de mantenimiento
|
|
> 1,4
|
90 -120
|
|
1,4 - 1,0
|
78 - 104
|
|
1,2 - 1,0
|
75 - 100
|
|
1,0 - 0,8
|
71 - 94
|
|
0,8 - 0,6
|
63 - 84
|
|
0,6 - 0,4
|
57 - 76
|
|
< 0,4
|
Tratamiento no recomendado
|
Tratamiento de mantenimiento: una infusión única diaria
de 2 horas de duración los 7 días de la semana en una dosis
comprendida entre 90-120 mg/kg si la función renal es normal (tabla
2).
Niños
El foscarnet se acumula en huesos y cartílagos. Los datos en animales
señalan que el acúmulo es mayor en animales jóvenes.
Dado que la seguridad del foscarnet en niños no ha sido investigada,
ni su efecto sobre el desarrollo del esqueleto, solo debe administrarse
en esta población cuando el beneficio potencial supere los posibles
riesgos.
Debe de administrarse únicamente por vía EV.
Vena periférica: una solución de la droga en una concentración
de 24 mg/mL, deberá de diluirse en dextrosa al 5 % o solución
salina fisiológica al 0,9 % en una concentración de 12 mg/mL.
Vena central: la solución de 24 mg/mL puede administrarse sin
dilución.
La toxicidad se reduce con la hidratación adecuada; por ello,
se recomienda añadir 0,5-1,0 litro de solución salina al
0,9 % a cada infusión intermitente.
Duración del tratamiento: inducción del tratamiento 2
a 3 semanas. El seguimiento dependerá de la respuesta clínica.
Al igual que el ganciclovir, debe restringirse el uso del foscarnet
a unidades especializadas con experiencia en su empleo.
CONTRAINDICACIONES
-
No administrar en enfermos tratados con pentamidina.
-
Hipersensibilidad al foscarnet.
-
No se recomienda su empleo en embarazadas o madres que lacten.
-
No se recomienda su empleo en pacientes con régimen de hemodiálisis.
EFECTOS SECUNDARIOS
-
Afectación de la función renal: aumento de azoados, disminución
del filtrado glomerular, insuficiencia renal aguda, acidosis metabólica.
-
Trastornos electrolíticos: hipocalcemia, hipomagnesemia, hipocaliemia,
hipofosfatemia, formación de quelatos con iones metálicos
(Ca, Mg, Fe, Zn).
-
Sistema nervioso central: ansiedad, nerviosismo, reacción agresiva,
psicosis, convulsiones.
-
Cardiovasculares: hipertensión, hipotensión, alteraciones
del ECG.
-
Otros: fiebre, astenia, fatiga, náuseas, vómitos, diarreas,
dispepsia, edemas en miembros inferiores, leucopenia, hemoglobina baja,
plaquetopenia, hemorragia, úlceras genitales, función hepática
anormal.
INTERACCIONES MEDICAMENTOSAS
-
Es incompatible con la dextrosa al 30 %, anfotericín B, aciclovir
sódico, ganciclovir, cotrimoxazol, vancomicina y soluciones que
contengan calcio.
-
Puede producir un efecto tóxico aditivo con otros fármacos
potencialmente nefrotóxicos (anfotericín B, pentamidina,
aminoglicósidos).
PRESENTACIÓN
Frasco de 250 mL; 1 mL = 24 mg (80 Fmol) = 6 g de foscarnet trisódico
hexahidrato.
IODOXURIDINA
Nucleósido tópico; fue uno de los primeros agentes antivirales
conocidos.36 A pesar de su uso amplio, brinda un beneficio pequeño
a pacientes con infecciones por herpes virus orolabial o genital. Su lugar
en las queratoconjuntivitis herpética ha sido suplantado hoy por
el aciclovir tópico. Se emplea en ungüento oftálmico
al 0,5 % 5 veces al día.
AMANTADINA/RIMANTADINA
AMANTADINA
INDICACIONES
Tiene actividad solamente contra el virus de la influenza A. Acorta la
duración de la fiebre y los síntomas respiratorios en pacientes
con influenza A si ésta es administrada dentro de las primeras 48
horas del comienzo de la enfermedad.37 También puede
ser usada profilácticamente en grupos de riesgo que no han sido
vacunados o en contactos no vacunados durante brotes epidémicos
en hospitales y otras instituciones.38
POSOLOGÍA
Profilaxis de la influenza A
Adultos y niños de 9 a 14 años: 100 mg cada 12 horas durante
10 días.
Niños de 1 a 9 años: 4,4 - 8,8 mg/kg/día dividido
en 2 ó 3 subdosis (máximo de 150 mg al día).
EFECTOS SECUNDARIOS
En general se considera poco tóxica
-
Trastornos neurológicos como ansiedad, insomnio, confusión
e incluso alucinaciones, principalmente en ancianos.
-
Deben evitarse actividades que requieran de la atención del individuo.
-
La amantadina se acumula en el organismo en pacientes con insuficiencia
renal.
-
Otras: náuseas, vómitos, hipotensión ortostática,
leucopenia (neutropenia), insuficiencia cardíaca.
RIMANTADINA
Es un análogo estructural de la amantadina, con el mismo espectro
de actividad e indicaciones clínicas. Es empleada en los países
que integraron la antigua Unión Soviética. Se plantea que
es más efectiva que la amantadina contra los virus tipo A de la
influenza a iguales concentraciones. Ésta se absorbe más
lentamente, por lo que alcanza niveles plasmáticos más bajos
y esto explica la presencia de menos manifestaciones de toxicidad.39
La eficacia de la rimantadina contra los virus de la influenza A ha sido
informada por estudios en la década de los años 80 por Dolin
y Quarles . Se presenta en tabletas de 50 mg.
VIDARABINA
Ha sido reconocida históricamente como la primera droga autorizada
a ser usada por vía sistémica en el tratamiento de las infecciones
virales. Se pensó en su eficacia para un grupo de infecciones por
herpes virus, incluyendo la encefalitis por HV, la infección neonatal
y el herpes zóster en huéspedes inmunodeprimidos. En la práctica
clínica actual la vidarabina ha sido desplazada ampliamente por
el aciclovir y sus derivados.
INDICACIONES
-
Actividad contra el virus herpes simple.
-
Actividad contra otros virus DNA particularmente varicela-zóster
y citomegalovirus.
POSOLOGÍA
Herpes neonatal: 30 mg/kg/día EV en infusión continua en
12 horas durante 10 días.
Queratitis por herpes virus: ungüento oftálmico 5 veces
al día.
Herpes zóster diseminado en pacientes inmunocomprometidos: 10
mg/kg/día EV en infusión continua en 12 horas durante 5 a
7 días.
RIBAVIRINA
Este análogo de nucleósido tiene actividad in vitro
contra un número determinado de virus RNA que incluyen el virus
sincitial respiratorio, virus de la influenza A, parainfluenza, parotiditis,
sarampión, el herpes simple y virus exóticos como el de la
fiebre Lassa.40 El fármaco administrado en aerosol presenta
absorción sistémica.
INDICACIONES
-
Infecciones graves del tracto respiratorio inferior por el virus sincitial
respiratorio en pacientes de alto riesgo (niños y lactantes con
enfermedad pulmonar crónica o con cardiopatías congénitas
o en prematuros). El tratamiento es efectivo cuando se inicia en los 3
primeros días. No se recomienda el uso de la ribavirina en aerosol
si no se ha identificado el agente causal.
-
Infecciones por influenza y parainfluenza en niños y adultos, aunque
su papel exacto en el tratamiento de estas enfermedades espera el resultado
de estudios futuros.
-
La ribavirina tiene un efecto beneficioso en los niveles de aminotransferasas
séricas y en los hallazgos histológicos hepáticos
en pacientes con hepatitis crónica por virus C, pero estos cambios
no se acompañan de mejora en los marcadores de RNA viral; por tanto,
su empleo como droga única por períodos prolongados (12 meses),
no tienen valor en el tratamiento de la hepatitis C.41
-
Ha sido aprobada para el tratamiento de la hepatitis crónica por
virus C en adultos combinados con el interferón.
POSOLOGÍA
-
Se administra exclusivamente en forma de aerosol con una concentración
final de 20 mg/mL, previa dilución con agua estéril.
-
El tratamiento se realiza durante 12 a 18 horas al día con un mínimo
de 3 días y un máximo de 7 en dependencia de la respuesta
clínica.
CONTRAINDICACIONES
-
No usarse en niños que requieran ventilación mecánica
asistida por la posible precipitación del fármaco en los
tubos y válvulas del respirador.
-
Las mujeres embarazadas o que puedan estarlo, y el personal de salud deben
adoptar precauciones especiales para disminuir la exposición a este
medicamento por su posible mutagenicidad y teratogenicidad.
EFECTOS SECUNDARIOS
-
Respiratorios: neumonía bacteriana, pneumotórax, apnea.
-
Cardiovasculares: paro cardíaco, hipotensión, intoxicación
por digital.
-
Hematológicas: la ribavirina se acumula en los hematíes y
puede producir una anemia hemolítica reversible con la retirada
del medicamento.
INTERACCIONES MEDICAMENTOSAS
A la solución final de ribavirina no se le debe agregar ningún
otro aditivo (broncodilatadores, esteroides, antimicrobianos, mucolíticos).
PRESENTACIÓN
Viale de 100 mL: ribavirina 6 g
INTERFERONES
Son una familia de sustancias naturales con efectos biológicos amplios.
El interferón alfa (IFN-a) tiene la mayor actividad antiviral.42
Ha sido estudiado principalmente como el tratamiento de las infecciones
crónicas por los virus de la hepatitis B y C, aunque puede ser usado
también para tratar infecciones debidas a otros virus, tales como
rinovirus, papilomavirus y retrovirus.
INDICACIONES
-
Hepatitis B. En más del 40 por ciento de los pacientes seleccionados
con hepatitis crónica por virus B, el tratamiento con IFN-a puede
conducir a la desaparición de la circulación del DNA de la
hepatitis (HBV), la DNA polimerasa y el antígeno e (Hbe), con mejoría
de las pruebas bioquímicas de función hepática y el
patrón hístico de la glándula. Los que responden,
por lo general se convierten en HbsAg negativos en controles seriados.43-45
Algunos factores como un anticuerpo HIV negativo, niveles séricos
bajos de DNA-HBV, niveles elevados de aminotransferasas y la inflamación
activa en la biopsia hepática, son predictores de una respuesta
favorable al interferón.
-
Hepatitis C. Adultos con hepatitis crónica C con anticuerpos anti-VHC
y elevación de la ALAT en suero sin insuficiencia hepática.
El 50 por ciento de los enfermos responden al IFN-a con normalización
de las enzimas hepáticas y mejoría morfológica en
las muestras biópsicas. Sin embargo, la mitad aproximadamente de
estos pacientes sufrirán recaídas una vez interrumpido el
tratamiento con el interferón-a. No se han identificado factores
de riesgo que aumenten la probabilidad de una respuesta favorable.
-
Papilomatosis laringo-traqueal. Es una enfermedad frecuente en niños
y adultos jóvenes en quienes papilomas escamosos recurren implacablemente
en la luz de la laringe y tráquea.
-
Condiloma acuminado.
POSOLOGÍA
Hepatitis crónica activa por virus B
No existe una pauta terapéutica óptima. Normalmente se usan
2,5 a 5 millones de UI/m2 de SC subcutánea, 3 veces por semana (aunque
algunas veces puede ser diaria) durante 6 a 12 meses. Si al cabo de 1 ó
2 meses de tratamiento no han disminuido los marcadores de multiplicación
viral o el Hbe, entonces puede aumentarse la dosis escalonadamente. Si
después de 4 meses de tratamiento no se observa mejoría,
considerar suspensión del mismo.
Una fase del tratamiento para la hepatitis B con IFN-a incluye su combinación
con otros agentes. La vidarabina y su derivado monofosfatado, así
como también el aciclovir han sido empleados con éxitos de
valor clínico relativo.46
También se ha sugerido que un ciclo corto de administración
de corticosteroides previo al tratamiento con IFN-a (prednisone priming),
produce un rebote inmunológico a partir de la retirada súbita
de la prednisona.47,48
Niños con hepatitis crónica B han recibido hasta 10 millones
de UI/m2 sin efectos secundarios importantes. Sin embargo, no se ha demostrado
la eficacia del tratamiento.34
Hepatitis crónica por virus C
La hepatitis por virus C es un problema de salud común en la población
adulta. Está indicado en pacientes con anticuerpos anti-!VHC, que
presenten elevación de ALAT sin descompensación de la función
hepática. No hay evidencia fehaciente de beneficio a largo plazo,
tanto en términos clínicos como histopatológicos.49
Dosis inicial: 6 a 9 millones de UI subcutáneas o IM 3 veces
por semana durante 3 meses como tratamiento de inducción.
Dosis de mantenimiento: Los pacientes que normalicen ALAT continuarán
con 3 millones de UI 3 veces por semana 3 meses más, aunque el lapso
puede extenderse hasta 11 a 12 meses.50 Los pacientes con ALAT
elevadas deben suspender el tratamiento.
La mayoría de los pacientes que recidivan tras recibir un tratamiento
adecuado, lo hacen en los 4 primeros meses después de suspender
el tratamiento.
Condiloma acuminado
Inyección intralesional (en la base de la verruga) de 1 millón
de UI de IFN-a recombinante 3 veces por semana durante 3 semanas produce
una respuesta aceptable.51
Papilomatosis del tracto respiratorio
El tratamiento estándar consiste en una escisión cuidadosa
microendoscópica, con un láser de dióxido de carbono.
En los últimos tiempos se ha informado del efecto benéfico
del IFN como coadyuvante del tratamiento quirúrgico.52,53
CONTRAINDICACIONES
-
Hipersensibilidad conocida al interferón o a cualquier componente.
-
Cardiopatía grave o historia de enfermedad cardíaca.
-
Insuficiencia renal, insuficiencia hepática, o disfunción
mieloide grave.
-
Hepatitis crónica con enfermedad hepática avanzada o cirrosis
hepática.
-
Hepatitis crónica en pacientes que recibían o han sido tratados
con inmunosupresores (excepto los casos con tratamientos breves con esteroides).
EFECTOS SECUNDARIOS
-
Síntomas generales: síntomas tipo influenza(fiebre, escalofríos,
mialgias, artralgias, diaforesis).
-
Síntomas digestivos: anorexia, náuseas, disgeusia, diarreas,
flatulencia.
-
Alteraciones de la función hepática: aumento de las transaminansas,
bilirrubina, deshidrogenasa láctica.
-
Raramente disfunción o insuficiencia hepática tras su administración.
-
Piel y mucosas: exantemas, exacerbacción de un herpes labial, sequedad
de la piel.Puede exacerbar o desencadenar una psoriasis.
-
Síntomas renales: nefritis intersticial (muy rara).
-
En transplantados renales o de médula ósea su acción
inmunoestimulantes puede reducir la eficacia de la inmunosupresión
terapéutica (ciclosporina).
-
Síntomas hematológicos: granulocitopenia, plaquetopenia,
anemia.
-
Síntomas neuropsiquiátricos: vértigos, visión
borrosa, somnolencia, impotencia transitoria, retinopatía isquémica,
neuropatía.
-
Puede afectar los reflejos y dificultar la ejecución de ciertos
trabajos como la conducción de vehículos y manejo de maquinarias
o equipos.
-
En ocasiones se ha observado comportamiento suicida en pacientes tratados
con interferón 2-a
PRESENTACIÓN
Bulbos de 3; 4,5; 9 o 18 millones de UI de interferón 2-a recombinante
liofilizado, 9 mg de cloruro de sodio y 5 mg de seroalbúmina humana.
RESISTENCIA VIRAL A LAS DROGAS
Los mecanismos de acción de las drogas antivirales y de la resistencia
a las mismas se conocen como elementos importantes, debido particularmente
a que son conocidas las estructuras cristalográficas a los rayos
X para numerosas proteínas diana virales. Esta resistencia habitualmente
incluyen sustituciones aminoacídicas en las proteínas diana
que evitan su unión a la droga o previene a una enzima de aceptar
el medicamento como un substrato. Esta información permite al médico
práctico un uso más efectivo de los agentes antivirales disponibles
y estimula el desarrollo de nuevas drogas.54
DESARROLLO DE NUEVOS MEDICAMENTOS DE ACCIÓN ANTIVIRAL
Los avances en la virología continúan la identificación
y definición en un nivel molecular de aquellos sitios de la multiplicación
viral que pueden ser vulnerables al ataque sin daño para la célula
hospedera. La caracterización completa de la DNA polimerasa viral,
necesaria para la duplicación del virus, pero no utilizadas por
la célula hospedera, es el objeto mayor de investigaciones en la
actualidad. De esta manera, numerosos agentes terapéuticos -mucho
de ellos análogos de nucleósidos! son evaluados sistemáticamente,
con el fin de identificar medicamentos de acción antiviral más
efectivos y menos tóxicos. Mencionaremos algunos de los más
prometedores: el famciclovir, valaciclovir y pensiclovir.55
FAMCICLOVIR
Es la forma absorbible por vía oral del agente antiherpes virus
penciclovir. Tiene una actividad potente y selectiva contra los herpes
virus. Estudios clínicos han demostrado que la droga es bien tolerada
por numerosos individuos a escala mundial.56,57
VALACICLOVIR
Se trata de un 1-valil éster del aciclovir; después de su
adiministración oral es convertido rápida y extensamente
en aciclovir a través de un metabolismo de primer paso.58
En el caso de la infección por el virus de la hepatitis B no
existe hasta el momento un tratamiento efectivo y seguro, y las investigaciones
clínicas sobre agentes antivirales prometedores como los análogos
de nucleósidos se encuentran limitadas por los efectos tóxicos
debidos a su distribución corporal específica.
Se dirigió el estudio hacia la posibilidad de emplear transportadores
activos de drogas antivirales hacia las células del parénquima
hepático, el sitio principal de multiplicación del VHB. Los
quilomicrones, quienes transportaron los líquidos a través
de receptores específicos de apoliproteína E, pudieran servir
como estos transportadores medicamentosos. Sin embargo, los de origen natural
dificultan su aplicación como drogas transportadoras famacéuticas,
por esto, la incorporación del análogo de nucleósido
iododeoxiuridina dentro de quilomicrones recombinantes, ofrece esperanza
de una actividad altamente selectiva hacia las células del parénquima
hepático, y representa un avance conceptual en el desarrollo de
un tratamiento efectivo y seguro para la hepatitis B.39
SUMMARY
We analyse mechanisms and sites of action of different agents and drugs
against those more frequent producing significant clinical and epidemiological
diseases. Development of molecular biology and advanced technologies, allow
knowledge of distinct stages of nucleic acids multiplications and viral
proteins; these steps may be critical points or targets, where chemical
substances of natural origin may act, or specially created by means of
improved techniques obstructing or even arrest viral replication. Main
goal of this paper is to familiarize physicians with this topic of little
practical application in our clinical setting. Antiviral therapy has arrived
to an era of progress that goes from therapeutical inability to present
possibility to treat many viral diseases. In a non distant future, physicians
must know about treatment of viral infections as well as the bacterial
ones.
Subject headings: ANTIVIRAL AGENTS/pharmacocinetics.
REFERENCIAS BIBLIOGRÁFICAS
-
Locarnini SA. Antiviral drugs: mechanism of action. Med Dig 1994;20(3):10-5.
-
Jackson GG, Rubinis M, Knigge M. Passive Inmunoneutralization of human
inmunodeficiency virus in patients with advanced AIDS. Lancet 1988;2:647.
-
Hannigan BM, Barnett YA, Armstrong DB, Mc Kelvey-Martin VJ, Mc Kenna PG.
Thymidime kinase: the enzimes and their clinical usefulness. Cancer Biother
1993;8(3):97.
-
Okada T, Guerney ME. Single basic amino acid substitutions at position
302 or 320 in the domain of HIV type 2 are not sufficient to alter the
antiviral activity of dextran sulfate and heparin. AIDS. Res Hum Retrovirus
1995;11(5):671-5.
-
Dalgleish AG, Beverly PCL, Claphan PR. The CD4 (T4) antigen is an essential
component of the receptor of the AIDS retrovirus. Nature 1984;312:763.
-
Mitsuya H, Looney DJ, Kuno S. Dextran sulphate suppression of viruses in
the HIV family. Inhibition of virion binding to CD4 + cells. Science 1988;240:646.
-
Klatzman D, Champagne E, Chamaret S. T-lymphocite T4 molecule Behaves as
the receptor for human retrovirus LAV. Nature 1984;312:767.
-
Davies WL, Grunert RR, Haff RF. Antiviral activity of 1-!ada-mantanamine
(amantadine). Science 1964;144:862-3.
-
Goldsmith S, Whitley RJ. Antiviral drugs. En: Gorbach SL, Bartlett JG,
Blacklow NR. Infectious Diseases: WB Saunders, Boston, 1992:289-302.
-
Schaeffer HJ, Beauchamp L, Miranda P de. 9- !(Hydroxyethoxymethyl) guanine
activity against viruses of the herpes group. Nature 1978; 272:583.
-
Elion GB, Furman PA, Fyre JE. Selectivity of action of an antitherapeutic
agent, 9(2-hidroxyethoxymethyl) guanine actvity. Proc Natl Acad Sci USA
1977;74:5716.
-
Gnam JW Jr, Barton NH, Whittley RJ. Acyclovir-mechanism of action, pharmacokinetics,
safety and clinical applications. Evaluations of new drugs. Pharmacotherapy
1983;3:275.
-
Dorsky DI, Crumpacker CS. Drug five years later: Acyclovir. Ann Intern
Med 1987;107:859.
-
Richman DD. Human inmunodeficiency virus antiviral therapy En: Gorbach
SL, Bartlett JG, Blacklow NR. Infectious Diseases: WB Saunders, Boston,
1992:977-98.
-
Blean B. Antiviral therapy: current concepts and practice. Clin Microbiol
Rev 1992;5:146-82.
-
Mc Laed GX, Hammer SM. Zidovudine: five years later. Ann Intern Med 1992;117:487-501.
-
Lipsky JJ. Zalcitabine and didanosine. Lancet 1993;341:30-2.
-
Matthews T, Boehme R. Antiviral activity and mechanism of action of ganciclovir.
Rev Infect Dis 1988;10(3):490.
-
Meyers JD. Management of cytomegalovirus infection. Am J Med 1988;10:S477.
-
Biron KK, Stenbuck PJ, Sorrell JB. Inhibition of the DNA poly-merases of
varicella-zoster virus and human cytomegalovirus by the nucleoside analogs
ACV and BW795U. J Cell Biochem 1984;8B:207.
-
Chatis PA, Miller CH, Schrager LE, Crumpacker CS. Sucessful treatment with
foscarnet of an acyclovir-resistant mucocutaneous infection with herpes
simplex virus in a patient with acquired inmunodeficiency syndrome. N Eng
J Med 1989;320:297.
-
Goldstein D, Lazzlo J. The role of interferon in cancer therapy: a current
perspective. Cáncer 1988;38:259.
-
Becker Y, ed. Antiviral drugs and interferon: the molecular Basis of Their
Activity. Boston: Martinus Nihoff, 1984:202.
-
Wray SK, Gilbert BE, Noall MW, Mode of action of ribavirin: effect of nucleotide
pool alterations on influenza virus ribonu-cleoprotein synthesis. Antiviral
Res 1985;5:29.
-
Eriksson BE, Helgtrand NG, Johnsson A. Inhibition of influenza virus ribonucleic
acid polymerase by ribavirin triphosphate. Antimicrob Agents Chemother
1977;11:946.
-
Hall CB, Mc Bride JT, Gala CL. Ribavirin greatment of respiratory syncytial
virus infection in infants with underlying cardiopulmonary disease. JAMA
1985;254:3047.
-
Shepp DH, Dandliker PS, Meyers JD. Treatment of varicella-!zoster virus
infection in severely inmunocompromised patients. N Engl J Med 1986;314:208.
-
Lundgren G, Wilczek H, Lonnqvist B. Acyclovir prophylaxis in bone marrow
trasplant receipients. Scand J Infect Dis 1985;47(Suppl): 137.
-
Wood MJ, Ogan PH, McKendrick MW. Efficacy of oral acyclovir treatment of
acute herpes zoster. Am J Med 1988;85:79.
-
Huff JC, Balfour HH, Laskin OL. Therapy of herpes zoster with oral acyclovir.
Am J Med 1988;85:84.
-
Pérez Ávila J, Ramos García A. Antivirales. Consideraciones
actuales. Rev Acta Méd 1990;4(2):268-83.
-
Erice A, Chou S, Biron KK. Progresive disease due to ganciclovir-resistant
citomegalovirus in inmunocompromised patients. N Engl J Med 1989;320:289.
-
Buhles WC, Mastre BJ, Tinkov AJ. Ganciclovir threatment of live-or sight-threatmentcytomegalovirus
infection experience in 134 immunocompromised patients. Rev Infect Dis
10 (Suppl):495, 1988.
-
BJ, Tinker AJ. Ganciclovir treatment of life-or sight-threatering cytomegalovirus
infection experience in 314 immunocompromised patients. Rev Infect Dis
1988;10(Suppl):495.
-
V-I Vademecum Internacional 36 ed. Madrid: MEDICUM, 1995: 956.
-
Rios F, Muñoz M, Spencer E. Antiviral activity of phosphonoformate
on rotavirus transcription and replication. Antiviral Res 1995;27(1-2):71-83.
-
Prussoff WM, Bakkle YS, Sekely A. Cellular and antiviral effects of halogenated
deoxyribonucleosides. Ann NY Acad Sci 1965;130:135.
-
Davies WL, Grunert RR, Haff RR. Antiviral activity of 1-!adamantanamina
(aamantadine). Science 1964;144:862-3.
-
Sears SD, Clements ML. Protective efficacy of low-dose amantadine in adults
challenged with wild -type influenza A virus. Antimicrob Agents Chemother
1987;31:1470.
-
Tominack RL, Hayden FG. Rimantadine hydrochloride and amantadine hydrochloride
use in influenza A virus infections. Infect Clin North Am 1987;1:459.
-
Mc Cormick JB, King IJ, Webb PA. Lassa fever. Effective therapy with ribavirin.
N Engl J Med 1986;314:20.
-
Di Bisceglie AM. Ribavirin as therapy for chronic hepatitis C. A randomized
double-blind, placebo-controled trial. Ann Intern Med 1995;123(12):887-893.
-
Lauta VM. Update on the use of interferons in clinical practice. Clin Ter
1995;146(6-7):393-448.
-
Greenberg HB, Pollard RB, Lutwick LI. Effect of human leukocyte interferon
on hepatitis B virus replication in patients with chronic active hepatitis.
N Engl J Med 1976;295:517.
-
Alexander GJM, Brahm J, Fagan EA. Loss of HBsAg with interferon therapy
in chronic hepatitis B virus infection. Lancet 1987;1:66.
-
Alexander GJM. Williams R. Natural history and therapy of chronic hepatitis
B virus infection. Am J Med 1988;85:143.
-
Hoofnagel J, Di Bisceglie A. Antiviral therapy of viral hepatitis. En:
Glasso G, Whitley R, Merigan T, eds; Antiviral agents and viral diseases
of man, ed 3. New York: Raven, 1987:187.
-
Hoofnagel J. Antiviral treatment of chronic type B hepatitis. Ann Intern
Med 1987;107:414.
-
Perrillo RP, Regenstein FG, Peters MG. Prednisone withdrawal followed by
recombinant a-interferon in the treatment of chronic non A, non B hepatitis.
N Engl J Med 1986;315:1575.
-
Hoofnagel JH, Mullen KM, Jones DB. Pilot study of recombinant human a-interferon
in chronic non-A, non B hepatitis. N Engl J Med 1986;315:1575.
-
Vanthiel DH, Friedlander L, Caraceni P, Molloy PJ, Kania RJ. Treatment
of hepatitis C virus in elderly person with interferon alpha. J Gerontol
A Biol Sci Med Sci 1995;50(6):M330!3.
-
Eron LJ, Judson F, Tucker S. Interferon therapy for condylomata acuminata.
N Engl J Med 1986;315:15:1059.
-
Haglund S, Judquist P, Cantell K, Strander H. Interferon therapy in juvenile
laryngeal paplillomatosis. Arch Otolaryngol 1981;107:327.
-
Goepfert J, Gutterman J, Dichtel W. Leukocyte interferon in patients with
juvenile papillomatosis. Ann Otol Rhino Laryngol 1982;91:431.
-
Richman DD. Drug resistance in viruses. Trends Microbiol 1994;2(10):401-7.
-
Nikkels AF, Pirard GE. Recognition and treatment of shingles. Drugs 1994;48(4):526-48.
-
Fowler SE, Pratt SK, LAroche J, Prince WT. Drug metabolism and Pharmacokinetics
interaction betwen oral famciclovir and allopurinol in healthy volunteers.
Eur J Clin Pharmaccol 1994;46(4):355-9.
-
Saltzman R, Jurewicz R, Boob R. Safety of famciclovir in patients with
herpes zoster and genital herpes. Antimicrob Agents Chemother 1994;38(10):2454-7.
-
Jacobson MA, Gallant J, Wang LH. Phase I trial of valaciclovir, the 1-valyl
ester of acyclovir, in patients with advanced human inmunodeficiency virus
disease. Antimicrob Agents Chemoter 1994;38(7):1534-40.
-
Rensen PC, Dijik Mcvan, Havenaar EC, Bijsterbosch MK, Kruijt JK, Berkel
TJvan. Selective liver targetin of antiviral by recombinant chylomicrons
- a new therapeutic approach to hepatitis B. Nat Med 1995;1(3):221-5.
Recibido: 11 de noviembre de 1997. Aprobado: 8 de diciembre de 1997. Lic.
Jesús Barreto Penié. Hospital Clinicoquirúrgico
"Hermanos Ameijeiras". San Lazaro No. 701 entre Belascoaín y Marqués
González, municipio Centro Habana, Ciudad de La Habana, Cuba.
1 Especialista de I Grado en Medicina
Interna.Máster en Nutrición.
2 Especialista de I Grado en Medicina Interna.Médico
intensivista.
3 Especialista de I Grado en Microbiología. Máster
en Infectología y Enfermedades tropicales.Médico intensivista.
4 Especialista de II Grado en Neumología.



