PRESENTACIÓN DE CASO
Enfermedad de Ménétrier
Ménétrier disease
Jesús Barreto Penié, Pedro Velbes Marquetti, Carlos Domínguez Álvarez, Kaly Cepero Llaugier, Zoilo Augusto Placeres León, Miguel Ángel Rodríguez Allende
Hospital Clínico Quirúrgico “Hermanos Ameijeiras”. La Habana, Cuba.
RESUMEN
La enfermedad de Ménétrier designa la coexistencia de hipertrofia de la mucosa gástrica, hipoclorhidria o hiperclorhidria e hipoproteinemia grave. El artículo se propone analizar las características clínicas, endoscópicas, imaginológicas, anatómicas e histopatológicas de un paciente atendido por presentar esta afección en el Hospital “Hermanos Ameijeiras” desde noviembre de 2014 hasta abril de 2015. Se realizó una evaluación y seguimiento interdisciplinario por gastroenterólogos, imaginólogos, hematólogos, cirujanos, patólogos y miembros del Servicio de Nutrición clínica. Después de solucionar los problemas nutricionales y una anemia grave, finalmente, se practicó una gastrectomía total con estenosis a nivel de la sutura esófago-yeyunal. Se resalta el tratamiento multidisciplinario e interdisciplinario aplicado al paciente, que resultó determinante en el resultado exitoso.
Palabras clave: enfermedad de Ménétrier; hipertrofia mucosa; desnutrición; hipoalbuminemia; carcinoma; gastrectomía.
ABSTRACT
Menetrier's disease designates the coexistence of hypertrophy of the gastric mucosa, hypochlorhydria or hyperchlorhydria and serious hypoalbuminemia. The article aims to analyze the clinical, endoscopic, imaginological, anatomical, and pathological characteristics of a patient who was treated at Hermanos Ameijeiras Hospital from November 2014 to April 2015. Gastroenterologists, radiologists, hematologists, surgeons, pathologists, and members of Clinical Nutrition Service performed interdisciplinary evaluation and monitoring. After solving nutritional problems and severe anemia, total gastrectomy was finally performed with stenosis at the level of the esophagus-jejunal suture. We highlight the multidisciplinary and interdisciplinary treatment applied to this patient, which proved crucial in the successful outcomes.
Keywords: Ménétrier disease; mucosal hypertrophy; malnutrition; hypoalbuminemia; carcinoma; gastrectomy.
INTRODUCCIÓN
En 1888, Pierre E. Ménétrier publicó por primera vez la relación existente entre gastropatía hipertrófica y el desarrollo de carcinoma gástrico. Tras su publicación se acuñó el término de enfermedad de Ménétrier (EM) para designar la coexistencia de hipertrofia de la mucosa gástrica, hipoclorhidria o hiperclorhidria, e hipoproteinemia grave, sin tener en cuenta la relación de esta con el desarrollo de cáncer gástrico. La EM es una variante muy infrecuente de gastropatía hiperplásica, caracterizada por la aparición de pliegues engrosados en la mucosa gástrica asociada a una pérdida de proteínas e hipoclorhidria.
La experiencia en el tratamiento quirúrgico de los pacientes con EM es reducida y se limita a los casos que cursan con hipoproteinemia grave o transformación maligna, sin embargo, la gastrectomía total debería indicarse como tratamiento definitivo en etapas más tempranas de la enfermedad.1 En el presente trabajo se analizan las características clínicas nutricionales, imaginológicas, endoscópicas, anatómicas e histológicas de un paciente diagnosticado y tratado quirúrgicamente por EM en el Hospital “Hermanos Ameijeiras”.
RESUMEN DE EXPEDIENTE CLÍNICO
Paciente AVV. Edad: 28 años. Sexo: masculino. Color de la piel: negra.
HC: 86071609E40. Nacionalidad: angolano.
Primer ingreso
Fecha de ingreso: 18/11/2014 Fecha de egreso: 27/11/2014. Estadía: 8 días
Servicio: Gastroenterología.
Motivo de ingreso: Diarreas y pérdida de peso.
HEA: Desde hace un año diarreas líquidas, amarillas, con restos de alimentos. Cólicos abdominales ocasionales, también náuseas y vómitos biliosos. Pérdida de 20 kg de peso. Se estudia bajo la hipótesis diagnóstica de enfermedad inflamatoria intestinal y/o linfoma con resultados negativos.
APP: Fiebre tifoidea.
Síntomas subjetivos (S/S): Borborigmos, aerocolia +++, deposiciones pastosas de 3-5 diarias, anorexia +++.
Síntomas objetivos (S/O). Disminución de depósitos grasos subcutáneos y atrofia muscular +++. Edemas en miembros inferiores hasta las rodillas +++. Peso habitual: 60 kg (2012) Peso actual: 42 kg; Talla: 1,71 m; IMC: 14,38 kg/m2. Por ciento de pérdida de peso reciente: 30.
Mucosas pálidas ++, húmedas. Hb: 86 g/L; Hto.: 031; albúmina sérica: 19,3 g/L; colesterol: 4,79 mmol/L.
Abdomen: Distendido, timpánico ++. Dolor a la palpación profunda de forma difusa. No visceromegalia ni masas visibles o palpables. RHA aumentados ++.
H1. Gastropatía hipertrófica tipo síndrome de Ménétrier
H2. Linfoma gástrico
Peso al egreso: 39 kg
Plan terapéutico (P/T):
1. Econutrición: Dieta BRATT (Banana, Rice, Apple, Tea, Toast)
2. Dietoterapia con 1,5 g de proteínas/kg de peso/día. Ovoalbúmina. Suplemento Nutricional Oral (SON) con fórmula polimérica hiperproteica (NUTRIAL). Sulfato de Zn 10 mg/día y ácido fólico 30 mg diarios
3. Bloqueador de bomba de protones, ansiolítico
Problemas de salud
Diagnóstico al egreso
Pr1. Enfermedad de Ménétrier
SPr 1,1. Desnutrición asociada a enfermedad crónica. Tipo mixta grave
Segundo ingreso
Fecha ingreso: 28/01/2015. Fecha egreso: 30/01/2015. Estadía: 2 días
Servicio: Cirugía general
MI: Diarreas y vómitos
Problemas de salud
Pr1. Enfermedad de Ménétrier
SPr 1,1. Desnutrición asociada a inanicióm. Tipo marasmo grave.
SPR 1,2. Anemia ferropénica grave. Testigo de Jehová
S/S. Se siente mejor, astenia ++. Diarreas aisladas. Cólicos y borborigmos +.
S/O. Peso: 42 kg. IMC: 14,38 kg/m2, Hb: 86 g/L Hto: 030. VCM: 76 fl. Albúmina sérica: 42 g/L. Colesterol: 4,65 mmol/L. Existe negativa del paciente para recibir tratamiento con hemoderivados EV por razones religiosas.
PT. El Servicio de Hematología recomendó administrar hierro parenteral preoperatorio. Dosis: 50 mg intramuscular 3 veces por semana con dosis total de 900 mg. Ácido fólico: 30 mg diarios por vía oral.
Tercer ingreso
Fecha de ingreso: 18/02/2015. Fecha de egreso: 19/02/2015. Estadía: 24 horas
Servicio: Cirugía general
MI: Diarreas y vómitos
Problemas de salud
Pr1. Enfermedad de Ménétrier
SPr 1,1. Desnutrición asociada a inanición. Tipo marasmo grave
SPR 1,2. Anemia ferropénica grave. Testigo de Jehová
Peso: 44 kg. No edemas. IMC: 14,87 kg/m2. Hb: 106 g/L; Hto: 036; VCM: 81 fl
PT. Se incorporaron simbióticos. Se propuso NPT perioperatoria
El Banco de Sangre sugirió el empleo de eritropoyetina recombinante. No se empleó por rechazo del paciente. Se mantuvo el Hierro Dextrán por vía IM profunda.
Cuarto ingreso
Fecha ingreso: 22/03/2015. Fecha egreso: 04/04/2015. Estadía: 12 días
MI: Para tratamiento quirúrgico
Problemas de salud
Pr1. Enfermedad de Ménétrier
SPr 1,1. Desnutrición asociada a inanición. Tipo marasmo moderado
SPr 1,2. Anemia ferropénica grave (resuelto). Testigo de Jehová
S/S. Dolor abdominal, diarreas, vómitos, borborigmos. Ingiere mejor alimentos y suplementos nutricionales. No pérdida de peso
S/O. Peso: 48 kg. No edemas. IMC: 16,27 kg/m2. Hb: 124 g/L; Hto 041; VCM: 91 fl
PT. 23/03/15. Gastrectomía total. Esófago-yeyunostomía y yeyunostomía alimentaria. No complicaciones. A las 48 horas se inicia alimentación-nutrición por acceso enteral con dietoterapia modificada en textura, ovoalbúmina, dieta polimérica hiperproteica (Nutrial), sulfato de Zinc, ácido fólico. Fumarato ferroso. Simbióticos. Vitaminoterapia por vía parenteral.
Se encontró estenosis a nivel de la sutura esófago-yeyunal sin fuga de contraste. Se inició vía oral sin dificultades a la semana de operado.
Ultrasonido abdomen (20/11/14)
Estómago con engrosamiento intenso de los pliegues. Ligera cantidad de líquido libre en su cavidad.
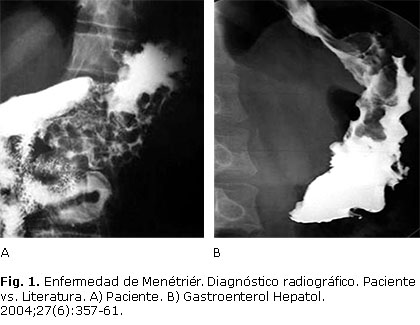
Rayos X de esófago, estómago y duodeno (21/11/2014) (Fig. 1)
Esófago: de aspecto normal.
Estómago: Pliegues gástricos engrosados en fundus, cuerpo y antro. No ulceraciones.
Duodeno: de aspecto normal.
Panendoscopia digestiva superior (24/11/14) (Fig. 2)
Estómago: Píloro central, pliegues engrosados que lo deforman parcialmente con eritema, edema y erosiones superficiales. Cuerpo y fundus muestran pliegues con características similares, muy engrosadas. Peristaltismo aumentado. Lago gástrico de contenido claro. Se toma biopsia.
Duodeno: Mucosa pálida que alterna con áreas de eritema.
Biopsia gástrica (26/11/14) (Fig. 3)
Gastritis crónica. Hiperplasia mucoide del epitelio de superficie y foveolar sugestiva de gastropatía hipertrófica (Enfermedad de Ménétrier).
(26/03/15) Biopsia de pieza anatómica (estómago) (Fig. 4)
Gastrectomía total. Gastropatía hipertrófica. Enfermedad de Ménétrier con afectación de toda la mucosa gástrica. No lesión en bordes de sección. Helicobacter pylori negativo.
(01/04/15) Se administró contraste hidrosoluble por VO. Esófago de aspecto normal con retardo en vaciado por estenosis a nivel de la sutura esófago-yeyunal con paso de contraste con dificultad. No fuga del contraste.
Las tablas 1 y 2 muestran los resultados de los estudios hemáticos y bioquímicos realizados en todos los ingresos del paciente.
DISCUSIÓN
La enfermedad de Ménétrier fue descrita por Pierre Ménétrier en 1888, se caracteriza por una hipertrofia gigante de la mucosa y la presencia de pliegues gástricos engrosados. Pertenece al grupo de las gastropatías hipertróficas, enfermedades infrecuentes caracterizadas por un crecimiento gigante y cerebriforme de los pliegues gástricos debido una hiperplasia epitelial sin inflamación. Se plantea que está relacionada con una liberación excesiva de factores de crecimiento.1-3
La mucosa gástrica afectada secreta cantidades masivas de mucina lo que conlleva a pérdida de proteínas acompañada de hipoalbuminemia y edema. Histológicamente se observa hiperplasia foveolar masiva asociada a una reducción de las glándulas oxínticas.2,4-7
La gastropatía hipertrófica (pliegues gástricos aumentados de tamaño) en el cuerpo gástrico se asoció con proliferación epitelial y pérdida de la diferenciación. Esta condición patológica eventualmente fue llamada enfermedad de Ménétrier. 8
Los criterios diagnósticos para esta rara enfermedad pueden presentarse parciales o incompletos. Un auténtico caso de EM es aquel que involucra:
1. Pliegues gigantes, especialmente en el fundus y cuerpo del estómago.
2. Hipoalbuminemia.
3. Hallazgos histopatológicos de hiperplasia foveolar, atrofia glandular e incremento del moco gástrico.
El diagnóstico de la enfermedad se basa en la sospecha clínica, la presencia en endoscopia e imágenes de pliegues gástricos engrosados y alteraciones histológicas características que incluyen hiperplasia foveolar, glándulas tortuosas y dilatadas, disminución de células parietales e infiltrado inflamatorio leve.9 La hipoclorhidria puede esperarse cuando el proceso involucra la mayoría de las glándulas mucosas del fundus.10
La forma adulta está asociada a una sobreexpresión del gen del factor transformador de crecimiento α (TGF-α), compromete típicamente el cuerpo y fondo gástrico respetando el antro.2,6,11
Es más frecuente en varones entre 50 y 60 años y se presenta clínicamente con dolor abdominal, náuseas, vómitos, pérdida de peso y edema periférico debido a la pérdida de proteínas dada por la excesiva secreción de mucina a través de la mucosa gástrica.2,7
La enfermedad compromete típicamente el cuerpo y fondo gástrico, respetando en general el antro. Existen reportes aislados en la literatura de compromiso gástrico difuso y solo dos señalan compromiso duodenal: en el primer caso se describe compromiso de fondo gástrico y de mucosa fúndica heterotópica a nivel duodenal, y en el segundo se describen lesiones difusas nodulares que afectan todo el estómago y duodeno proximal, confirmándose histológicamente enfermedad de Ménétrier.12
El hallazgo histológico por excelencia es un intenso y tortuoso crecimiento foveolar, que puede estar relacionado con dilatación quística prominente. Dichos quistes pueden penetrar la muscularis mucosae y extenderse a la submucosa. La lámina propia es muy edematosa, algunas veces pierden la proliferación fibroblástica, y contienen un número incrementado de eosinófilos y células mononucleares, especialmente foveolares. La superficie y el epitelio foveolar pueden exhibir hallazgos compatibles con gastritis linfocítica.13
Junto a la intensa hiperplasia foveolar existe una disminución en el número de glándulas fúndicas, que se reemplazan por glándulas mucosas (metaplasia pseudopilórica).8
La pérdida de proteínas ocurre a través de esta mucosa anormal, ya sea por vía de las úlceras superficiales comúnmente presentes, o como consecuencia de una linfangiectasia submucosa8
La EM se diagnostica usualmente después de la quinta década de la vida, es más común en el sexo masculino, y, en raras ocasiones, puede mostrar predisposición familiar.14
El espectro clínico es amplio. Dentro de los hallazgos más comunes se encuentran: dolor epigástrico, pérdida de peso, anemia, diarrea y edema, síntomas presentes en el paciente presentado. Este último puede ser la forma inicial de presentación.15 Estos hallazgos fueron descubiertos en autopsias de individuos con carcinoma gástrico.
La causa de la EM se desconoce. Se han postulado factores infecciosos como Citomegalovirus y H. pylori que participarían principalmente en la forma infantil, habitualmente reversible en forma espontánea o secundario al tratamiento de la infección.16,17
La EM se ha informado también en niños, pero es muy probable que no se trate de la misma enfermedad, debido a que es reversible y se asocia a la infección por Citomegalovirus (CMV). Algunos autores sugieren el abandono del término Enfermedad de Ménétrier en niños, en caso de determinarse aumento de tamaño de pliegues gástricos y que no se identifique infección por CMV, en estos casos se prefiere el término gastropatía hipertrófica indeterminada; mientras que en aquellos con gastropatía hipertrófica e infección por CMV se emplearía el término gastropatía por Citomegalovirus. En los últimos años se ha relacionado también con la infección por Helicobacter pylori,18 sobre todo en adultos, como en los casos reportados por Santaloria Piedrahita y colaboradores.19 En el caso que se presenta el paciente tuvo prueba de Helicobacter pylori negativa en la biopsia.
Desde el punto de vista de laboratorio, la anormalidad característica es un nivel bajo de albúmina y niveles bajos de proteínas séricas totales. El pico de liberación de ácido se ha reportado en un intervalo de 10 mM/h, pero la hipoclorhidria no es un hallazgo universal, por tanto, aunque los estudios para determinar la secreción ácida son interesantes en esta enfermedad, no se requieren para hacer el diagnóstico .
En radiografías con bario, los pliegues pueden observarse aumentados de tamaño, nodulares y tortuosos e incluso pueden observarse cráteres entre ellos. La figura 1 muestra el estudio radiográfico del estómago del paciente.
También se ha mencionado el empleo del ultrasonido transabdominal como modalidad diagnóstica no invasiva en el caso de pliegues gástricos gigantes.20
La endosonografía abdominal constituye una herramienta útil para el diagnóstico diferencial, pues permite evaluar las características de los pliegues gástricos engrosados, apoyando el diagnóstico de EM cuando el engrosamiento se origina en la mucosa profunda.21 La endoscopia confirmó los hallazgos del estudio baritado y pudo revelar, incluso, erosiones superficiales y úlceras (Fig. 2).
Las biopsias endoscópicas pueden no ser representativas de toda la mucosa, revelando solo hiperplasia foveolar, la cual sugiere el diagnóstico pero no lo confirma.
El diagnóstico definitivo requiere la demostración de hiperplasia foveolar acompañada por pérdida importante de glándulas fúndicas y cambios quísticos, y para esto, algunos autores mencionan la biopsia por laparotomía como única forma de establecer el diagnóstico definitivo.11
El diagnóstico diferencial debe considerar enfermedades gástricas que puedan causar engrosamiento de pliegues como síndromes polipósicos con compromiso gástrico, pólipos hiperplásicos, síndrome Cronkhitee Canada, linitis plástica y linfoma. 2,22 .
El tratamiento de la enfermedad se basa principalmente en el tratamiento quirúrgico, especialmente en pacientes con pérdida no controlable de proteínas y debido al posible riesgo de malignización.23 El paciente en cuestión calificó en todos esos criterios.
En los casos asociados a infección por H. pylori o Citomegalovirus se ha comunicado el control parcial de los síntomas luego del tratamiento de la infección. Se han utilizado tratamientos empíricos con antiácidos, anticolinérgicos, octreótido y prednisona, sin embargo, no existen evidencias sólidas de beneficios asociados a estas terapias.6,9,24 La información acerca del pronóstico y seguimiento es limitada. Algunos pacientes con úlceras o erosiones asociadas pueden beneficiarse sintomatológicamente con terapia para úlcera péptica.25 Aquellos pacientes con pocos síntomas e hipoalbuminemia mínima no requieren terapia específica. Se han sugerido regresión de síntomas y recuperación de la hipoalbuminemia e incluso algunos mencionan desaparición de la hipertrofia de los pliegues gástricos, seguidos de terapias que incluyen anticolinérgicos, antiácidos, antibióticos,26 en los que la erradicación de H. pylori fue seguida por mejora de los síntomas y resolución de la hipoalbuminemia, sugiriendo que si se comprueba la presencia de H. pylori la primera línea de tratamiento consiste en terapia de erradicación y antiinflamatorios.19 Pese a estos resultados se considera que la cura de la EM no es la conducta conservadora, debido a que se han visto complicaciones durante el tratamiento y una frecuencia considerable de degeneración carcinomatosa que aparece tarde o temprano,1,27 de aquí, que se considere a la gastrectomía como estrategia de curación definitiva, aunque estrictamente hablando se prefiere realizarla en aquellos pacientes que presentan una enfermedad grave, esto sería en caso de síntomas abdominales persistentes como vómito y náusea, e hipoalbuminemia.10 La forma localizada en el estómago distal se cura con resección subtotal del estómago; la forma difusa y aquella que se localiza en el estómago proximal, con gastrectomía total.27
Los resultados del tratamiento quirúrgico se informan regularmente como favorables, pero existen reportes de recurrencia en el estómago residual en el caso de la gastrectomía subtotal. La pérdida de un tratamiento médico adecuado se suplementa por la terapia quirúrgica con gastrectomía total o parcial. El tratamiento es necesario siempre y cuando la pérdida proteica se considere como riesgo elevado para la vida.
La muerte puede ocurrir como resultado de la hipoproteinemia o la hipoglucemia dada por el cáncer en sí. El cáncer gástrico también se ha descrito como parte del diagnóstico o durante el seguimiento de los pacientes con EM.28
La enfermedad se ha asociado a mayor riesgo de cáncer gástrico, pero la magnitud de este riesgo es incierta y oscila entre 0-10 % en la literatura.29,30
La resección gástrica es aún el tratamiento más efectivo para la enfermedad, pero la extensión apropiada de la resección aún no ha sido determinada. Uno de los factores de mayor peso a la hora de determinar la extensión de la resección gástrica en la EM es su potencial maligno.1,31 Se ha sugerido que la gastropatía hiperplásica localizada podría ser un indicador de un incremento en el riesgo para tumores gastrointestinales en general, más que como una lesión posiblemente premaligna por sí misma. Existen varios reportes de pacientes en los que histológicamente se prueba gastropatía hiperplásica de las células productoras de moco o del tipo mixto, en las que el adenocarcinoma fue diagnosticado varios años después.32
Una cuestión no resuelta es la extensión de la gastrectomía. Los partidarios de la gastrectomía total la defienden porque con ella se elimina el riesgo de malignización, la localización es fúndica y se obvia la realización de una anastomosis con una mucosa hipertrofiada.31 Por el contrario, los defensores de una intervención quirúrgica más conservadora por menos extensa, afirman que esta permitiría controlar los síntomas con menor morbilidad. Quizá la postura más razonable sea adaptar la técnica a la localización de la EM y el grado de displasia celular. Así, en los casos difusos, localizados cerca del cardias ─como ocurre habitualmente─, o con displasia, neoplasia o ambas, la gastrectomía total es la técnica preferida (Fig. 4), mientras que en las lesiones antrales sin signos de displasia, una gastrectomía subtotal puede ser suficiente.
Algunos autores catalogan a la EM como una enfermedad rara, un desorden premaligno adquirido del estómago, de origen desconocido. Se ha informado sobre enfermos de carcinoma, algunos incidentalmente al tiempo del diagnóstico o durante el curso de la enfermedad, y se ha sugerido tanto como condición precancerosa en sí como diagnóstico asociado.
Se ha descrito la transformación carcinomatosa de la mucosa fuera del área de hiperplasia; llama la atención que en todos el tumor fue detectado en un estadio temprano. La proporción inusualmente alta de carcinomas superficiales (pT1) no es sencillo de explicar, aunque podría ser porque inducen síntomas clínicos tempranos que facilitan el diagnóstico, o que el tipo de carcinoma que surge tiene un potencial bajo de progresión.32 Se ha mencionado incluso, un caso en el que la mucosa hiperplásica se localizaba distal al adenocarcinoma ulcerado, sin embargo, también se ha observado adenocarcinoma superficial que surge a partir del área de hiperplasia, lo cual indica que la gastropatía hiperplásica de las células productoras de moco o del tipo mixto, pueden guardar relación como una condición que indica un incremento en el riesgo de carcinoma gástrico en general, más que como una posible lesión precancerosa por sí misma. Esto afecta la manera en la que la gastroscopia y el examen patológico y biopsias deben dirigirse.32
Se ha pensado también en la influencia de la transformación del factor de crecimiento alfa en la mucosa gástrica (TGF-α Transforming Growth Factor-alpha en inglés). La forma adulta está asociada a una sobreexpresión del gen TGF-α, compromete típicamente el cuerpo y fondo gástrico respetando el antro.2,6 Se ha encontrado cierta relación entre el aumento del TGF-α que inhibe la secreción gástrica, estimula migración y proliferación celular a nivel de la mucosa gástrica y aumenta los niveles de mucina gástrica, y la patogénesis y el estatus premaligno de la EM. Se ha encontrado que la infección por H. pylori se asocia fuertemente a la presencia del alelo TNFA-857 T, la gastritis hipertrófica y la promoción de carcinoma.33
La demostración del trastorno de señalización asociado al receptor del factor de crecimiento epidérmico (EGFR en inglés) en la EM ha permitido el tratamiento con cetuximab, anticuerpo monoclonal que bloquea el sitio de unión del EGFR, con 7 casos comunicados en la literatura con respuesta favorable.34-36 Sin embargo, el uso de cetuximab aún es considerado como tratamiento “compasivo” por parte de la Food and Drugs Administration de Estados Unidos (FDA), por lo que el tratamiento de elección para la EM continúa siendo la gastrectomía total o parcial según el compromiso gástrico presente y las características clínicas. En el caso de nuestro paciente se realizó gastrectomía total dada la severidad de la enfermedad.
Una característica distintiva en este paciente fue la coexistencia de una anemia grave de tipo ferropénica. Por su origen africano y raza afroide, se investigaron otras posibles hipótesis diagnósticas, especialmente hemoglobinopatías: talasemia, siclemia; parasitismo intestinal u otras causas de anemia, también el déficit de precursores de la hemoglobina como la cobalamina y el ácido fólico. Otro detalle que interfirió con la solución definitiva (la intervención quirúrgica programada), fue que el paciente profesaba la fe religiosa de los “Testigos de Jehová”, quienes tienen prohibido el uso de sangre y hemoderivados. Ante la imposibilidad de poder emplear eritropoyetina recombinante, se acudió al método tradicional de administrar sales de hierro parenteral siguiendo las recomendaciones del Formulario Nacional de Medicamentos del MINSAP, con resultado exitoso a mediano plazo.37 Nutricionalmente, el paciente presentó una desnutrición de tipo mixta con predominio del marasmo, pues dominaba el mecanismo de la inanición, por ingesta deficiente y malabsorción combinadas. La hipoalbuminemia y los edemas, respondieron más a la enteritis perdedora de proteínas que a un cuadro de kwashiorkor con presencia de inflamación grave. Finalmente, no se halló una explicación plausible a la elevación importante de los niveles de fosfatasa alcalina hepática; la literatura revisada tampoco describe este hallazgo relacionado con la EM.
Hasta el momento de esta revisión, el paciente se encuentra asintomático en su país de origen y lleva una vida normal, con las limitaciones dietoterapéuticas que le impone una gastrectomía total (síndrome de dumping inicial, riesgo de anemia por déficit de hierro y de vitamina B12).
CONCLUSIONES
El diagnóstico de la EM y la estrategia terapéutica que se decida seguir con estos pacientes se debe apoyar en una colaboración interdisciplinaria entre imagenólogos, gastroenterólogos, patólogos y cirujanos, e incluso personal de biología molecular, lo que representa la posibilidad de mejorar los resultados y aminorar el riesgo de neoplasias en este grupo de enfermos.28,38
En la actualidad la publicación de casos clínicos supone una importante herramienta docente con aplicaciones prácticas y contribuyen a la expansión del conocimiento entre los profesionales de la salud.39
REFERENCIAS BIBLIOGRÁFICAS
1. Miriam N, García-Álvarez NM, Plata-Muñoz JJ, Medina-Franco H. Gastrectomía total en el manejo de la enfermedad de Ménétrier. Experiencia institucional y revisión de la literatura. Rev Gastroenterol Mex. 2007;72(3):244-8.
2. Coffey R, Washington M, Corless C, Heinrich M. Ménétrier disease and gastrointestinal stromal tumors: hyperproliferative disorders of the stomach. J Clin Invest. 2007;117(1):70-80.
3. Gompertz M, Montenegro C, Bufadel ME, Defilippi C, Castillo J, Morales C. Enfermedad de Ménétrier con compromiso gástrico difuso y duodenal. Caso clínico. Rev Med Chile. 2012;140:1174-8.
4. Lambreht N. Ménétrier´s disease of the stomach: a clinical challenge. Curr Gastroenterol Rep. 2011;13:513-7.
5. Ramia JM, Sancho E, Lozano O, Santos JM, Domínguez F. Enfermedad de Ménétrier y cáncer gástrico. Cir Esp. 2007;81 (3):153-4.
6. Famularo G, Sajeva MR, Gasbarrone L. Beyond gastritis and before cancer: the strange case of Ménétrier’s disease. Intern Emerg Med. 2011;6(4):369-71.
7. Rich A, Zuluaga T, Tanksley J, Fiske W, Lind C, Ayers G et al. Distinguishing Ménétrier’s disease from its mimics. Gut. 2010;59(12):1617-24.
8. Sleisenger M, Fordtran J, Scharschmidt B, Feeldman M. Gastrointestinal disease. Pathophysiology/diagnosis/management. 10ma. ed. Vol. 1. Philadelphia: Editorial Saunders; 2016. p. 881-3.
9. Lambreht N. Ménétrier´s disease of the stomach: a clinical challenge. Curr Gastroenterol Rep. 2011;13:513-7.
10. Settle SH,Washington K,Lind C,Itzkowitz S,Fiske WH, Burdick JS, et al. Chronic treatment of Menetrier’s disease with Erbitux: clinical efficacy and insight into pathophysiology. Clin Gastroenterol Hepatol. 2005;3:654-9.
11. Gompertz M, Montenegro C, Bufadel ME, Defilippi C, Castillo J, Morales C. Enfermedad de Ménétrier con compromiso gástrico difuso y duodenal. Caso clínico. Rev Med Chile. 2012;140:1174-8.
12. Wu CS, Lin CJ, Chen TC, Chen PC, Chiu CC. Ménétrier’s disease: a new variant with duodenal involvement. Am J Gastroenterol. 1997;92(6):1041-3.
13. Kim J, Cheong JH, Chen J, Hyung WJ, Choi SH, Noh SH.. Menetrier’s disease in Korea: report of two cases and review of cases in a gastric cancer prevalent region. Yonsei. Med J. 2004;30(45):555-60.
14. Dykes CM. Ménetrier’s disease: Case study in the quality of life. Gastroenterol Nurs. 2003;26:3-6.
15. Wilkerson ML, Meschter SC, Brown RE. Menetrier’s disease presenting with iron deficiency anemia. Ann Clin Lab Sci. 1998;28:14-8.
16. Megged O, Schlesinger Y. Cytomegalovirus-associated protein-losing gastropathy in childhood. Eur J Pediatr. 2008;167(11):1217-20.
17. Fretzayas A, Moustaki M, Alexopoulou E, Nicolaidou P. Menetrier’s disease associated with Helicobacter pylori: three cases with sonographic findings and a literature review. Ann Trop Paediatr. 2011;31(2):141-7.
18. Watanabe K, Beinborn M, Nagamatsu S, Ishida H, Takahashi S. . Menetrier’s disease in a patient with Helicobacter pylori infection is linked to elevated glucagons-like-peptide-2 activity. Scand J Gastroenterol. 2005; 40:477-81.
19. Santolaria Piedrafita S, Conde García R, Abascal Agorreta M, Domínguez Torres I, Ducóns García J, Guirao Larrañaga R, Montoro Huguet M. Resolution of Menetrier’s disease after eradication of Helicobacter pylori infection. Gastroenterol Hepatol. 2004;27:357-61.
20. Okanobu H, Hata J, Haruma K, Hara M, Nakamura K, Tanaka S, Chayama K. Giant gastric folds: differential diagnosis at US. Radiology. 2003;226:686-90.
21. Hizawa K, Kawasaki M, Yao T, Aoyagi K, Suekane H, Kawakubo K, et al. Endoscopic ultrasound features of protein-losing gastropathy with hypertrophic gastric folds. Endoscopy. 2000;32 (5):394-7.
22. Rich A, Zuluaga T, Tanksley J, Fiske W, Lind C, Ayers G et al. Distinguishing Ménétrier’s disease from its mimics. Gut. 2010;59(12):1617-24.
23. García-Alvarez MN, Plata-Muñoz JJ, Medina-Franco H. Total gastrectomy in the management of Ménétrie’s disease. Institutional experience and review of the literature. Rev Gastroenterol Mex. 2007;(72):244-9.
24. Burdick JS, Chung EK, Thinner E, Ster M, Paciga JE, Cheng JQ, et al. Treatment of Ménétrier's disease with a monoclonal antibody against epidermical growth factor receptor. New Engl J Med. 2000;343:1697-701.
25. Schulz J, Kohler B, Wegener K, Riemann JF, Me-enétrier’s disease-a rare cause of a protein deficiency syndrome, Dtsch Med Wochenschr. 1992;3(117):531-4.
26. Raderer M, Oberhuber G, Templ E, Wagner L, Pötzi R, Wrba F, et al. Successful symptomatic management of a patient with Ménétrier’s disease with long-term antibiotic treatment. Digestion. 1999;60:358-62.
27. Mattig H, Mahnke W. Localized Ménétrier disease and stomach cancer. Dtsch Z Verdau Stoffwechselkr. 1984;44:67-76.
28. Dykes CM. Ménétrier’s disease: Case study in the quality of life. Gastroenterol Nurs. 2003;26:3-6.
29. Ramia JM, Sancho E, Lozano O, Santos JM, Domínguez F. Enfermedad de Ménétrier y cáncer gástrico. Cir Esp. 2007;81(3):153-4.
30. Pereyra L, Gómez E, Mella J, Casas G, Bugari G, Cimmino D, et al. Diffuse gastric cancer associated with Ménétrier’s disease. Acta Gastroenterol Latinoam. 2011;41(2):142-5.
31. Kim J, Cheong JH, Chen J, Hyung WJ, Choi SH, Noh SH. Ménétrier’s disease in Korea: report of two cases and review of cases in a gastric cancer prevalent region. Yonsei. Med J. 2004;30(45):555-60.
32. Stamm B. Localized hiperplastic gastropathy of the mucous cell- and mixed cell-type (localized Ménétrier’s disease): a report of 11 patients. Am J Surg Pathol. 1997;21:1334-42.
33. Ohyama I, Ohmiya N, Niwa Y, Shirai K, Taguchi A, Itoh A, et al. The association between tumour necrosis factor-alpha gene polymorphism and the susceptibility to rugal hyperplastic gastritis and gastric carcinoma. Eur J Gastroenterol Hepatol. 2004 Jul;16(7):693-700.
34. Burdick JS, Chung EK, Thinner E, Ster M, Paciga JE, Cheng JQ, et al. Treatment of Ménétrier’s disease with a monoclonal antibody against epidermical growth factor receptor. New Engl J Med. 2000;343(23):1697-701.
35. Nalle S, Turner J. Ménétrier’s disease therapy: rebooting mucosal signaling. Sci Transl Med. 2009;1(8):8-10.
36. Fiske W, Tanksley J, Nam K, Goldenring J, Slebos R, Liebler DC, et al. Efficacy of Cetuximab in the treatment of Ménétrier’s disease. Sci Transl Med. 2009;1(8):11-8.
37. Ministerio de Salud Pública de Cuba. Formulario Nacional de Medicamentos 4ta. ed. La Habana: Editorial Ciencias Médicas; 2014. p. 357-8.
38. Melita P, Calbo L, Cucinotta E, Gorgone S, Palmeri R, Pergolizzi FP, et al. Gastric precancerous conditions. Chir Ital. 1995;47:54-8.
39. Martínez Martínez G, Noreña AL, Martínez Sanz JM, Ortiz Moncada R. Revisión metodológica para escribir y publicar casos clínicos: aplicaciones en el ámbito de la nutrición. Nutr Hosp. 2015;32(5):1894-1908.
Recibido: 4 de marzo de 2016.
Aprobado: 11 de junio de 2016.
Jesús Barreto Penié. Hospital "Hermanos Ameijeiras". Correo electrónico: penie@infomed.sld.cu