ARTÍCULO ORIGINAL
Facofragmentación continua en la catarata senil con núcleos de diversa consistencia
Continuous phacofragmentation in senile cataract with nuclei of different consistencies
Dr. Francisco Rey García González, Dra. Dayamí Pérez Gómez, Dra. Ester Novoa Sánchez
Hospital Clínico Quirúrgico "Hermanos Amejeiras". La Habana, Cuba.
RESUMEN
Se evaluó la utilidad de la facofragmentación continua en núcleos de diversa consistencia. Mediante un estudio descriptivo, prospectivo y longitudinal en 82 pacientes con catarata senil sin enfermedad ocular concomitante, operados de abril de 2007 a abril de 2008. Se evaluaron la agudeza visual, el astigmatismo, la tensión ocular, la morfología del endotelio corneal y la relación entre la consistencia nuclear intraoperatoria y los datos preoperatorios. La edad fue 62 ± 10 años. El 84,3 % de los núcleos fueron de consistencia semidura y dura. La agudeza visual con corrección fue 0,92 ± 0,08 al sexto mes. Aumentó la consistencia nuclear según aumentaron: la coloración nuclear, la edad y la disminución del reflejo rojo naranja. La facofragmentación continua es una técnica útil y segura para emulsificar cristalinos de mayor dureza, es innecesaria en los blandos y semiblandos y deficiente en los ultraduros al incrementarse el tiempo y la energía de ultrasonido.
Palabras clave: técnicas de facoemulsificación, consistencia nuclear, facofragmentación continua.
ABSTRACT
Usefulness of continuous phacofragmentation with nuclei of different consistency was evaluated by means of a descriptive, prospective and longitudinal study which was conducted in 82 patients with senile cataract without concomitant ocular disease who underwent surgery from April 2007 to April 2008. Visual acuity, astigmatism, ocular tension, morphology of cornel endothelium and the relation between intraoperative nuclear consistency and the preoperative data were evaluated. The age was 62 +/- 10 years. The 84, 3 % of the nuclei were of both medium-hard and hard consistency. Visual acuity with correction 6 months after was 0, 92 ± 0, 08. Consistency of the nucleus increased as nuclear coloration, the age, and the decrease of orange-red reflex increased. Continuous phacofragmentation is a useful and safe technique for emulsifying lens of great hardness; it is not necessary in soft and semi-soft ones and it is inefficient in the ultra- hard ones since the time and energy of the ultrasound is increased.
Key words: phacoemulsification techniques, consistency of the nucleus, continuous phacofermentation.
INTRODUCCIÓN
La facoemulsificación (FACO) es una variante de extracción extracapsular del cristalino basada en el empleo de vibraciones ultrasónicas para emulsificarlo y extraerlo por una incisión pequeña. No es una novedad. Fue presentada hace más de treinta años por el Dr. Charles Kelman. En las últimas décadas la FACO ha sido aceptada de forma generalizada entre los oftalmólogos.
Esta aceptación está basada en que el empleo de vibraciones ultrasónicas, la irrigación-aspiración controlada y la pequeña incisión proporcionan ventajas sustanciales, que la hacen una técnica segura por: el control total de la presión intraocular durante la cirugía que reduce la posibilidad de las complicaciones clásicas, la oportunidad de proseguir con la cirugía del segmento posterior inmediatamente después de la extracción de la catarata que nos deja un ojo fuerte e intacto con visualización clara hacia la cavidad vítrea, la rehabilitación visual en el posoperatorio inmediato con aumento de la agudeza visual (AV) importante, el astigmatismo corneal bajo debido a la pequeña incisión (2,8-3,2 mm), sin suturas o con un número reducido de ellas que se comporta como astigmáticamente neutra.1
La FACO ha evolucionado desde la emulsificación inicial en la cámara anterior a la actual, en saco capsular (in situ), en la cámara posterior o en el plano del iris que permite remover el núcleo central duro, antes que el epinúcleo y la corteza. Este cambio estuvo influenciado por el reconocimiento de que la masa nuclear de lentes firmes y duros podía dividirse en pequeños pedazos, para una remoción controlada dentro de la concha protectora del epinúcleo y que una apertura capsular producida por una capsulorrexis circular continua anterior (CCCA) resistiría las fuerzas implicadas en la división nuclear, lo que aumenta el margen de seguridad para la FACO.1
Este principio de dividir la masa nuclear es el que ha permitido evolucionar de la FACO inicial con fuertes poderes ultrasónicos a la actual con un uso más racional de la energía ultrasónica regulando a la vez los parámetros de flujo y vacío junto a la aparición de una variedad de técnicas adecuadas a la consistencia blanda, mediana, dura o muy dura del núcleo.2 La emulsificación del núcleo puede realizarse con técnicas de fractura (cracking) o sin fractura (non cracking). La técnica Chip and Flip de Fine es un ejemplo entre las técnicas sin fractura. Las técnicas de fractura pueden agruparse en dos categorías: en la primera se encuentran las que buscan líneas naturales de falla dentro del cristalino y lo fragmentan a través de ellas, por ejemplo: técnica de Phaco chop de Nagahara, el Stop and Chop, el Cracking y el Pre-chop; en la segunda se encuentran las que crean surcos específicos preestablecidos para abrir grietas y subdividir el cristalino en cuadrantes, por ejemplo: el Divide y Vencerás (Divide and Conquer) de Gimbel. A partir de la técnica de Phaco chop de Nagahara, David Chang ha promovido una denominada non stop Phaco chop (Phaco chop continuo o facofragmentación continua) que constituye una de las variantes, con el objetivo de aumentar el espectro de cataratas operables con FACO. La eficiencia de la facofragmentación continua estriba en que toda la fuerza se dirige a favor de las fibras del cristalino, seccionando el núcleo con movimientos de separación mecánica con un chopper sin energía ultrasónica, esta es sustituida por energía manual al subdividir el núcleo y se utiliza solo para facilitar la aspiración de trozos nucleares. Se ha demostrado el menor empleo de energía ultrasónica del phaco chop en comparación con las otras técnicas de FACO.1-3 Esta reducción combinada de poder, tiempo de FACO y estrés de la zónula disminuye el potencial de pérdida de células endoteliales, y hace que la facofragmentación continua sea ventajosa en núcleos duros, donde hay menos epinúcleo para proteger la cápsula posterior de estas fuerzas y movimientos, que siendo hacia adentro también evitan la posibilidad y extensión de desgarros anteriores periféricos a la cápsula posterior. También es muy ventajosa al enfrentarnos a casos de alto riesgo con córneas seniles, pupilas pequeñas de 4 mm o menos, zónulas débiles (pseudoexfoliación), cataratas traumáticas, cataratas maduras e hipermaduras y núcleos brunescentes.1-5
La prometedora utilidad de la facofragmentación continua asociada a la gran cantidad de pacientes que acuden a la consulta con cataratas avanzadas, ha sido el fundamento de este estudio, en el que se intenta evaluar esta técnica en la catarata senil con núcleos de diversa consistencia y la relación entre la consistencia nuclear intraoperatoria y parámetros clínicos preoperatorios.
MÉTODOS
En el Servicio de Oftalmología del hospital "Hermanos Ameijeiras" se realizó un estudio prospectivo, descriptivo y longitudinal en 82 pacientes con diagnóstico de catarata senil y agudeza visual con corrección de 0,6 o menor que no padecieran ninguna enfermedad ocular concomitante, a quienes se les realizó cirugía de catarata por facofragmentación continua, después de solicitar su consentimiento informado para participar en el estudio, entre los meses de abril de 2007 y abril de 2008. Se estudiaron la agudeza visual, el astigmatismo posoperatorio, la tensión ocular, la morfología del endotelio corneal y la relación entre la consistencia nuclear intraoperatoria y los datos clínicos preoperatorios, se describió la frecuencia de accidentes intraoperatorios, las complicaciones posoperatorias y el tiempo de rehabilitación visual.
Los pacientes se clasificaron según los siguientes parámetros del examen oftalmológico:
- Reflejo rojo-naranja:
ausente o presente de intensidad fuerte, débil o intermedia (entre fuerte
y débil). Según la intensidad con que se aprecia este reflejo
a la oftalmoscopia a distancia.
- Color de
la catarata: amarillo claro, amarillo intermedio, amarillo fuerte, broncíneo,
cobrizo y pardo. Según clasificación de los autores basada en
trabajos previos (3).
- Morfología
de la catarata: subcapsular, cortical, nuclear o la combinación de las
anteriores.
Durante la cirugía se clasificó el grado de dureza del núcleo del cristalino en: núcleo blando, semiblando, semiduro, duro o ultraduro, definiéndose según la proporción ascendente de la fuerza necesaria para el corte manual (táctil) con el segundo instrumento y el porciento de energía máxima de ultrasonido (US).
En el postoperatorio los pacientes se evaluaron a las 24 h, 1 semana, 1 mes, 2 meses y 6 meses. Se tomó como tiempo de rehabilitación visual aquel que transcurrió desde realizada la operación hasta que el paciente alcanzó una agudeza visual de 0,6 a 1 con corrección, estable.
Para evaluar los resultados se utilizó el test de t de Student para muestras pareadas y se consideró que dichos cambios fueron significativos cuando la probabilidad asociada al test fue menor de 0,05.
RESULTADOS
Se operaron 82 pacientes de ellos 51 (62,2 %) fueron mujeres y 31 (37,8%) hombres con edad de 62 ± 10 años oscilando entre 43 y 81 años.
Durante la cirugía de identificó la consistencia nuclear observándose que 3 (3,7 %) núcleos fueron blandos, 7 (8,5 %) fueron semiblandos, 38 (46,3 %) semiduros, 32 (39,1 %) duros y 2 (2,4 %) ultraduros.
Se logró realizar la técnica de facofragmentación continua en todos los núcleos duros (n.32), en todos los núcleos semiduros (n.38) y en los semiblandos que tuvieron reflejo de fondo débil (n.2) y eran de morfología nuclear (n.2), no se logró realizar la técnica en los semiblandos (n.7).
El tiempo de FACO fue de 1,32 ± 0,72 minutos (rango 0,39-3,50). El porciento de energía de ultrasonido máxima empleada fue de 54% ± 6. La agudeza visual con corrección preoperatoria fue de 0,35 ± 0,18 (rango 0,05-0,6) y la posoperatoria al sexto mes de 0,92 ± 0,08 (rango 0,6-1), p.001. El astigmatismo corneal preoperatorio fue de 0,87 ± 1,07 D (rango 0-4,5) y el astigmatismo corneal residual al sexto mes fue de 0.75 D ± 0,53 D (rango 0.25 -2,00), p .03. El tiempo de rehabilitación visual fue de 29 ±3 días (rango 7-21 días).
La tensión ocular fue en el preoperatorio de 17,52 ±3,29 mm Hg (rango12-23) y en el posoperatorio al mes de 14,83 ± 2,52 mm Hg (rango10-21), p= 0,001. La morfología del endotelio corneal mostró pleomorfismo y polimegatismo en el 54 % de la muestra preoperatoria y en el 100 % en el posoperatorio al sexto mes, además de la aparición de un espacio acelular en 2 pacientes (6 %). La pérdida de células endoteliales fue de 7 % (2350 / mm2 a 2185 / mm2).
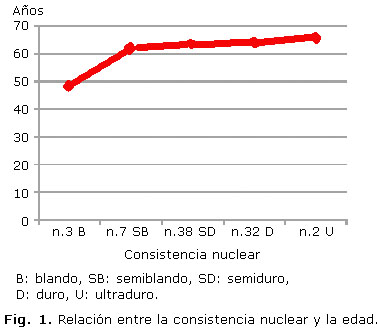
La edad en los pacientes con núcleos blandos fue de 47,67 ± 4,04 años; en los núcleos semiblandos fue de 61,29 ± 5,41 años; en los semiduros de 62,71 ± 9,19 años; en los duros de 63,44 ± 10,88 años y en los ultra duros de 65 ±1,41 años (Fig. 1).
Con respecto a la relación consistencia nuclear intraoperatoria e intensidad del reflejo de fondo observamos que en los núcleos blandos (B) la intensidad preoperatoria del reflejo rojo naranja fue intermedia en los 3 casos (100 %); en los semiblandos (SB) fue intermedia en 5 (71,4 %) y débil en 2 (28,6 %); en los semiduros (SD) fue intermedia en 17 (44,7 %) , débil en 17 (44,7 %) y ausente en 4 (10,6 %); en los duros (D) fue intermedia en 1 (3,1 %), débil en 17 (84,4 %) y ausente en 4 (12,5 %); en los ultraduros (UD) fue débil en 1 caso (50 %) y ausente en el otro (50 %) (Fig. 2).
Al observar la coloración de los núcleos en el examen preoperatorio en lámpara de hendidura fueron de color amarillo claro 14 (17,1 %), amarillo intermedio 49 (59,8 %), amarillo oscuro 16 (19,5 %) y broncíneo 3 (3,6 %).
Cuando se relacionó la consistencia nuclear identificada en el intraoperatorio y la coloración nuclear observada en el preoperatorio vimos que los núcleos blandos fueron de color amarillo claro en el 100 % (n.3). Los semiblandos fueron amarillo claro en 71,4 % (n.5) y amarillo intermedio en el 28,6 % (n.2). Los núcleos semiduros fueron amarillo claro en el 15,8 % (6), amarillo intermedio en el 81,6 % (n.31) y amarillo oscuro en el 2,6 % (n.1). Los de consistencia dura fueron amarillo intermedio en el 50 % (n.16), amarillo oscuro en el 44 % (n.14) y broncíneo en el 6 % (n.2). Los ultraduros fueron 1 (50 %) amarillo oscuro y 1 (50 %) broncíneo (Fig. 3).
Al relacionar la consistencia nuclear con la morfología de la catarata, de los núcleos blandos 2 (66,6 %) fueron subcapsulares posterior y 1 (33,3 %) corticonuclear, de los semiblandos 2 (28,6 %) fueron subcapsulares posteriores y 5 (71,4 %) nucleares, de los semiduros 4 (10,5 %) fueron subcapsulares posteriores, 14 (36,8 %) corticonucleares y 20 (52,6 %) nucleares, de los duros 14 (43,7 %) fueron corticonucleares y 18 (56,3%) nucleares y de los ultraduros 2 (100%) fueron nucleares (tabla).
Las complicaciones intraoperatorias presentadas fueron: la lesión térmica de iris en 4 ojos (4,8 %), la ruptura de cápsula posterior en 3 ojos (3,6 %), la desinserción capsular en 2 ojos (2,4 %).
Las complicaciones posoperatorias inmediatas (primera semana) fueron: el edema corneal transitorio en 17 ojos (20,7 %), los pliegues de la Descemet en 11 ojos (13,4 %), la reacción fibrinoide en área pupilar en 2 ojos (2,4 %) y la iridociclitis leve en 2 ojos (2,4 %).
Las complicaciones posoperatorias mediatas (de 1 semana a 1 mes) fueron: el edema corneal en 1 ojo (1,2 %), los pliegues de la Descemet en 2 ojos (2,4 %), la iridociclitis leve en 2 ojos (2,4 %) y la opacidad de cápsula posterior en 1 ojo (1,2 %). Las complicaciones posoperatorias tardías (después de 1 mes a 6 meses) fueron: la iridociclitis leve en 1 ojo (1,2 %), la vitritis en 1 ojo (1,2 %), la atrofia sectorial de iris en 4 ojos (4,8 %), las sinequias posteriores en 1 ojo (1,2 %) y la opacidad de cápsula posterior en 3 ojos (3,7 %).
DISCUSIÓN
La mayoría de los núcleos fueron de consistencia semidura o dura, lo que refleja el predominio de cataratas de gran consistencia entre la edad promedio de los pacientes que acuden a estas consultas. En la experiencia de los autores la realización de la facofragmentación continua en núcleos de consistencia blanda y semiblanda fue muy difícil por la poca resistencia que ofreció el núcleo a la punta de FACO que impidió realizar el empalamiento paracentral inicial, fue necesario disminuir los parámetros de vacío y poder de ultrasonido para evitar aspirar y traspasar el núcleo. Otra característica del empleo de esta técnica en los núcleos de menor consistencia fue la dificultad para lograr la rotación nuclear, la fractura en mitades y la fragmentación en cuñas por su naturaleza blanda. En cambio, en los núcleos de consistencia semidura y dura sí se obtuvo el empalado inicial y se logró la sucesiva bisección nuclear y la fragmentación en cuñas, que fueron emulsificadas y aspiradas. Los núcleos ultraduros fueron abordados aumentando fragmentación y los niveles de vacío y flujo, aunque en ellos es difícil la fragmentación por la naturaleza elástica de las fibras cristalinianas.
En este medio donde la mayor parte de los pacientes con catarata senil presentan núcleos de consistencias duras y semiduras aumenta la utilidad de la técnica como señalan varios autores, con predominio de cataratas avanzadas en sus consultas, al considerar que las técnicas de fragmentación son más útiles para núcleos de mayor dureza pues se sustituye la energía ultrasónica por la energía mecánica, se reduce el estrés zonular y se libera menor energía calórica dentro del ojo con la consiguiente reducción de las complicaciones postoperatorias, aunque las cataratas más duras ofrecen más retos y tienen mayor tendencia a generar complicaciones intra y posoperatorias.1-6
El tiempo medio de FACO y el porciento de ultrasonido empleado con la facofragmentación continua fueron similares al de la bibliografía revisada. Demostrando que estas técnicas requieren menor tiempo y energía de ultrasonido.6-10 El tiempo de facofragmentación nuclear continua fue breve.
La agudeza visual con corrección preoperatoria mejoró sustancialmente en el posoperatorio, fue muy significativa la diferencia entre la media inicial de 0,35 y la media postoperatoria de 0,92 con valores similares al de otros artículos revisados.6,11-13 La diferencia entre el astigmatismo corneal preoperatorio y el inducido fue significativa con un valor medio preoperatorio de 0,87 ± 1,07 D y posoperatorio de 1,39 ± 1,23 D supuestamente debido a la ampliación de la incisión corneal inicial de 3,2 mm hasta 6,5 mm para la implantación de un lente intraocular rígido de PMMA (óptica 5,25-7 mm). El tiempo medio de rehabilitación visual fue de 29 ± 3 días, momento en el cual se indicó la corrección óptica lo que resultó muy ventajoso para los pacientes en edad laboral, este resultado es común en este tipo de cirugía de la catarata que permite una rehabilitación visual rápida y una reincorporación precoz a las actividades habituales del paciente. Otros autores observaron similares resultados lo que está relacionado con una de las mayores ventajas de la FACO, su pequeña incisión que garantiza buenos resultados refractivos inmediatos.7-12
Respecto a la tensión ocular se observó una disminución significativa entre la media preoperatoria (17,52 ± 3,29 mm Hg.) y la posoperatoria al mes (14,83 ± 2,52 mm Hg), descenso parecido al señalado en otros artículos publicados.14-17
El porciento de pérdida de células endoteliales observado (7 %) concuerda con los valores que se reflejan en diferentes publicaciones, los autores coinciden en observar que con los adelantos de la técnica quirúrgica, el uso correcto del viscoelástico y el cuidado en optimizar las funciones del equipo de FACO se consigue una menor disminución de las células endoteliales.18-20
Al relacionar la consistencia nuclear y una serie de parámetros clínicos preoperatorios se encontró que: aunque existe una tendencia al aumento de la edad media de los pacientes en los grupos de dureza nuclear creciente, solo fue significativa la diferencia de edad entre los núcleos de consistencia blanda con el resto de las consistencias, fue de menor edad en los blandos en comparación con el resto de los grupos (Fig. 1). La intensidad del reflejo rojo naranja (fuerte, intermedio débil o ausente) decreció con el aumento de la consistencia: entre los blandos y semiblandos prevaleció el reflejo intermedio, en los núcleos semiduros y duros sobresalió el reflejo intermedio y débil, con algunos ausentes y en los núcleos ultra duros el reflejo fue débil o ausente (Fig. 2). La coloración de los núcleos en relación con su consistencia reveló un aumento a medida que aumentaba la dureza nuclear, fueron los núcleos blandos y semiblandos de color amarillo claro mayormente, los semiduros de color amarillo intermedio predominantemente, los duros tanto de color amarillo intermedio como amarillo oscuro casi en su totalidad y los ultraduros amarillo oscuro o broncíneo. Más de las tres cuartas partes de los núcleos fueron de color amarillo intermedio y amarillo oscuro, correspondiéndose con consistencias semiduras y duras esencialmente. Mientras que menos de una cuarta parte fueron de color amarillo claro, que se correspondió con consistencias blandas o semiblandas en más de la mitad (Fig. 3). En la relación de la morfología de la catarata con la consistencia nuclear creciente se apreció que en las cataratas subcapsulares posteriores no hubo ningún núcleo duro ni ultraduro en cambio en las cataratas con componente nuclear prevalecieron los semiduros y duros (tabla). Otros autores han descrito también una estrecha relación entre la dureza nuclear y su coloración, observando de forma general resultados similares.19-25 Los accidentes intraoperatorios y las complicaciones postoperatorias no fueron frecuentes pero si comunes al desarrollo de la FACO como se ha reportado en las publicaciones revisadas.25-29
La facofragmentación continua es una técnica útil para núcleos de consistencia semidura y dura, innecesaria e ineficiente para núcleos blandos y semiblandos que no fracturan. En los núcleos ultraduros se hará deficiente en la medida que se incremente el tiempo y la energía de FACO a emplear. Ofrece satisfactorios resultados de la agudeza visual corregida, el astigmatismo inducido, la tensión ocular y el estado de las células endoteliales en el posoperatorio, proporcionando una rápida rehabilitación visual. La consistencia nuclear se incrementa con la edad y el aumento de la coloración es directamente proporcional al aumento de la consistencia. La frecuencia de accidentes intraoperatorios y las complicaciones posoperatorias inherentes a la técnica quirúrgica es baja, considerándose una técnica segura.
REFERENCIAS BIBLIOGRÁFICAS
1. Bascom Palmer Eye Institute. Las perlas del XIX Curso Interamericano de Oftalmología Clínica. Miami, USA: Ciba; 1997.
2. American Academy of Ophthalmology. Basic and Clinical Science Course. Lens and cataract. USA: American Academy of Ophthalmology; 2010-11.
3. García F, Camacho F, Novoa E. Relación entre la coloración y la consistencia nuclear en la catarata senil. San Francisco: American Academy of Ophthalmology and Pan-American Academy of Ophthalmology Meeting; 1999.
4. Escaf LJ, Tello A, Rojas V, Castro A. Sistema de clasificación por grados de las cataratas programadas para facoemulsificación. Centurión V. En: El Cristalino de las Américas. Sao Paulo: Livraria Santos editorial; 2007. p. 51-61.
5. Kamoi K, Mochizuki M. Phaco forward-chop technique for managing posterior nuclear plate of hard cataract. J Cataract Refract Surg. 2010;36(1):9-12.
6. Kamoi K, Mochizuki M. Phaco forward-chop technique fo managing posterior nuclear plate of hard cataract. J Cataract Refract Surg. 2010 Jan;36(1):9-12.
6. Zeng M, Liu X, Zhang X, Xia Y, Liu Y, Yuan Z, et al. A comparative study of non-chopping rotation and axial rotation versus quick chop phacoemulsification techniques. Ophthalmic Surg Lasers Imaging. 2009 May-Jun;40(3):222-31.
7. Curbelo L, Río M, Hernández J, Capote A, Pérez E, Fernández G, et al. Integración del facochop en la moderna cirugía de cataratas: técnica de multichop. Instituto Cubano de Oftalmología "Ramón Pando Ferrer". Rev Cubana Oftalmol. 2006;19(1).
8. Wong T, Hingorani M, Lee V. Phacoemulsification time and power requirements in phaco chop and divide and conquer nucleofractis techniques. J Cataract Refreact Surg. 2000 Sep;26(9):374-8.
9. DeBry P, Olson RJ, Crandall AS. Comparison of energy required for phacochop and divide and conquer phacoemulsification. J Cataract Refract Surg. 1998 Nov;24(5):689-92.
10. Park JH, Lee SM, Kwon JW, Kim MK, Hyon JY, Wee WR, et al. Ultrasound energy in phacoemulsification: a comparative analysis of phaco-chop and stop-and-chop techniques according to the degree of nuclear density. Ophthalmic Surg Lasers Imaging. 2010 Mar-Apr;41(2):236-41.
11. Laudanska-Olszewska I, Synder A, Wesolek-Czernik A, Omulecki W. Comparison of efficacy and safety of cataract phacoemulsification in patients with different degree of nuclear sclerosis. Klin Oczna. 2008;110(4-6):172-5.
12. Joshi MR, Shakya S. Change in refractive status of the patients undergoing phacoemulsification surgery. Nepal Med Coll J. 2009 Mar;11(1):19-22.
13. Wilczynska O, Wilczynski M, Omulecki W. Surgically induced astigmatism after bimanual phacoemulsification through microincision and after standard phacoemulsification. Klin Oczna. 2010;112(4-6):115-9.
14. Jamil AZ, Iqbal K, Ur Rahman F, Mirza KA. Effect of phacoemulsification on intraocular pressure. J Coll Physicians Surg Pak. 2011 Jun;21(6):347-50.
15. Salima B, Andalloussi I, Fouad C, Khadija D, Hicham T. Changes in intraocular pressure after clear corneal phacoemulsification in normal patients. Oman J Ophthalmol. 2009 Sep-Dec; 2(3):1113.
16. Irak-Dersu I, Nilson C, Zabriskie N, Durcan J, Spencer HJ, Crandall A. Intraocular pressure change after temporal clear corneal phacoemulsification in normal eyes. Acta Ophthalmol. 2010 Feb;88(1):131-4. Epub 2009 Sep 16.
17. Wei-Wen Su, Phil Yeong-Fung Chen, Ching-Hsi Hsiao. Primary Phacoemulsification and Intraocular Lens Implantation for Acute Primary Angle-Closure. PLoS One. 2011; 6(5):e20056.
18. Rosado-Adames N, Afshari NA. The changing fate of the corneal endothelium in cataract surgery. Curr Opin Ophthalmol. 2012 Jan;23(1):3-6.
19. Bansal A. Endothelial cell damage with phacoemulsification techniques. J Cataract Refract Surg. 2009 Feb;35(2):213.
20. Storr-Paulsen A, Norregaard JC, Ahmed S, Storr-Paulsen T, Pedersen TH. Endothelial cell damage after cataract surgery: divide-and-conquer versus phaco-chop technique. J Cataract Refract Surg. 2008 Jun;34(6):996-1000.
21. Smith JM, El-Brawany M, Nassiri D, Tabandeh H, Thompson GM. The relationship between nuclear colour and opalescence on the LOCSIII scale and physical characteristics of cataract nuclei. Eye. 2002 Sep;16(5):543-51.
22. Kim JS, Chung SH, Joo ChK. Clinical application of a Scheimpflug system for lens density measurements in phacoemulsification. J Cataract Refract Surg. 2009;35(7):120-49.
23. Gullaspalli VK, Murthy PR, Murthy KR. Colour of the nucleus as a marker of nuclear hardness diameter and central thickness. Indian J Ophthalmol 1995 Dec;43(4):181-4.
24.Tabandeh H, Thompson GM, Heyworh P. Lens hardness in mature cataracts. Eye. 1994;8:453-5.
25. Heyworth P, Thompson GM, Tabandeh H, Mc Guigans. The relationship between clinical classification of cataract and lens hardness. Eye. 1993;7:726-30.
26. Ruchi Goel, Saurabh Kamal, Sushil Kumar, Jugal Kishore, et al. Feasibility and Complications between Phacoemulsification and Manual Small Incision Surgery in Subluxated Cataract. J Ophthalmol. 2012:205139.
27. Hugkulstone CE. Standing phacoemulsification: a prospective audit of 20 consecutive cases. J Cataract Refract Surg. 2010 Oct;36(10):1763-7. Epub 2010 Jul 31.
28. Ahmet Taylan Yazici, Ercument Bozkurt, Necip Kara, Yusuf Yildirim, Ahmet Demirok, Omer Faruk Yilmaz. Long-Term Results of Phacoemulsification Combined with Primary Posterior Curvilinear Capsulorhexis in Adults. Middle East Afr J Ophthalmol. 2012 Jan-Mar;19(1):115-9.
29. Vinay Agarwal, Jinish Upadhyay. Validation of scoring system for preoperative stratification of intra-operative risks of complications during cataract surgery: Indian multi-centric study. Indian Cataract Risk Stratification Study group. Indian J Ophthalmol. 2009 May-Jun;57(3):21-35.
Recibido:
Aprobado:
Francisco Rey García González. Hospital Clínico Quirúrgico "Hermanos Amejeiras". San Lázaro No. 701 entre Belascoaín y Marqués González, Centro Habana. La Habana, Cuba. CP 10 300. Autor para la correspondencia: Dra. Dayamí Pérez Gómez. Correo electrónico: dayione@infomed.sld.cu