ARTÍCULO DE REVISIÓN
Infección Asociada a la Atención de Salud
Liodelvio Martínez Fernández, Héctor Manuel Díaz Torres
Hospital Hermanos Ameijeiras. Habana. Cuba.
RESUMEN
La Infección Asociada a la Atención de Salud se define como la infección que ocurre después de la admisión hospitalaria y que no estaba presente ni incubándose en ese momento. Se asocia a una elevada morbilidad y mortalidad, inconveniencias sustanciales para el paciente y la institución, así como un alarmante incremento en el costo de la atención y cuidados de estos pacientes para la institución. Ellas incluyen a una lista diversa como la infección del sitio quirúrgico, infección del tracto urinario, neumonía y la infección del torrente sanguíneo. Se han desarrollado, adoptado y probado múltiples políticas y regulaciones en un intento de reducir el impacto de estas Infección Asociada a la Atención de Salud. Esta revisión se enfoca en los principales aspectos de la historia y tipos de Infección Asociada a la Atención de Salud, así como las medidas para su control.
Palabras clave: infección y atención de salud; infección hospitalaria; infección nosocomial; infección del torrente sanguíneo por catéter endovascular; infección del sitio quirúrgico; infección del tracto urinario, neumonía asociada a la ventilación mecánica.
ABSTRACT
Healthcare-associated infection are defined as infections developing after hospitalization or stay at a healthcare facility that were not present or incubating at the time of admission. It has been associated with increasing morbidity and mortality, substantial inconvenience for the patient and institution, as well as striking increases in the cost of care of those patients for the institution. They encompass a diverse list including skin and surgical site infections, urinary tract infections, pneumonia and blood stream infections. Many policies and regulations have been developed, adopted and tested in an attempt to decrease the impact of these healthcare-associated infection. In this review we addressed the main aspects of the history and types of healthcare-associated infection, as well as the measures to control them.
Keywords: healthcare infection; hospital acquired infection; nosocomial infection; catheter-related bloodstream infection; surgical site infection; urinary tract infections; ventilator-associated pneumonia.
INTRODUCCIÓN
La infección nosocomial se refiere a las infecciones asociadas a la atención de salud y viene de la palabra griega nosocomium, que significa hospital. Se define como la infección que ocurre después de la admisión hospitalaria y que no estaba presente ni incubándose en ese momento. Debido al creciente manejo ambulatorio de la prestación de servicios de salud, por ejemplo, la quimioterapia y la cirugía ambulatoria, el término de infección asociada a la hospitalización ha disminuido y se ha adoptado el de “Infección Asociada a la Atención de Salud” (IAAS). Se asocia a una elevada morbilidad y mortalidad, inconveniencias sustanciales para el paciente y la institución, así como un alarmante incremento en el costo de la atención y cuidados de estos pacientes para la institución.1
HISTORIA
Los hospitales europeos de la edad media eran considerados como lugares de almacenamiento de personas con enfermedades intratables donde eran cuidados hasta su fallecimiento. Estas enfermedades en su mayoría eran infecciosas, por lo que debido al característico hacinamiento de los pacientes, ocurría su contagio como regla. En el siglo XIX las intervenciones quirúrgicas casi siempre se infectaban y el 60 % de las amputaciones de extremidades se infectaban y daban al traste con la vida.
El descubrimiento y rápida aplicación de los agentes antibacterianos tales como las sulfonamidas y la penicilina en la tercera y cuarta décadas del siglo pasado fue presagiado como un milagro médico y trajo como consecuencias una reducción de las tasas de infección quirúrgica. Sin embargo, estos avances fueron seguidos por la aparición de IAAS por bacterias resistentes a estos antibióticos. El primer aislamiento de Staphylococcus aureus penicilino-resistente (SAPR) fue realizado en el momento del descubrimiento de la penicilina y en poco tiempo, una pandemia de infecciones nosocomiales por este agente motivó la realización de reuniones internacionales que llevaron a la creación de programas de control de la infección hospitalaria. El surgimiento de otras intervenciones de salud salvadoras de vida fueron seguidas a su vez de la aparición de nuevos tipos letales de infecciones como la septicemia por catéteres endovasculares, la endocarditis de válvulas protésicas y la neumonía asociada a la ventilación mecánica.
En la década de los 70 se hizo más frecuente la IAAS causada por bacilos gramnegativos, pero en los 80 retornó el predominio de la afección por cocos grampositivos, siendo el Staphylococcus aureus y el Staphylococcus coagulasa negativa los que desarrollaron niveles elevados de resistencia a las nuevas drogas desarrolladas para combatir estas infecciones como la Meticillina y otros betalactámicos. En los 90 emergió el enterococo vancomicina resistente, particularmente en los enfermos inmunodeficientes y ya en la década pasada emergieron como patógenos significativos los bacilos gramnegativos multidrogoresistentes,2 lo que se ha visto favorecido por el surgimiento de nuevas modalidades terapéuticas que implican el desarrollo de un estado de inmunodepresión como la quimioterapia y los trasplantes de órganos.
IMPORTANCIA
En la década de los 70 del siglo anterior se describía la afectación por este tipo de infección entre el 6 y el 8 % de los pacientes admitidos en el hospital. En los 90 esto cambió poco, pero la reducción de la admisión de pacientes en los hospitales debido el incremento de la realización de acciones de salud en forma ambulatoria hizo que en realidad se incrementase el problema y en realidad la hospitalización de personas en peores condiciones de salud provocó un incremento sustancial.
La IAAS provoca inconveniencia adicional a los pacientes, sufrimiento, invalidez y mortalidad en estos pacientes. También causan prolongación de la hospitalización, y un significativo incremento en los costos de la atención,3 provocando afectación del sistema de salud a tal punto que en los EUA se estima el costo anual promedio de estas infecciones entre 28,4 y 45 billones de USD y causan como promedio una prolongación de la estadía hospitalaria en 7 días con un costo de 40 890 USD adicionales para aquellos que sobreviven a la estadía en la Unidad de Cuidados Intensivos.
RESERVORIOS Y TRANSMISIÓN DE LAS IAAS
Las IAAS pueden ocurrir por varias razones y son producidas por una multitud de patógenos. Primeramente debe mencionarse a la que ocurre en pacientes severamente inmunocomprometidos ya sea por una enfermedad de base o por medidas terapéuticas en los que un microbio que raramente produce una infección, puede colonizar y finalmente infectar a un paciente hospitalizado. En segundo lugar debe mencionarse que la hospitalización y los procedimientos diagnósticos o terapéuticos asociados a ella pueden brindarle al patógeno acceso a partes del cuerpo que normalmente están protegidas. Por ejemplo, la inserción de un catéter percutáneo a través de la piel provee de una puerta de entrada al torrente sanguíneo. En tercer lugar debemos mencionar que otros patógenos no se encuentran en el hospedero en el momento del ingreso y sólo lo colonizan después del mismo, frecuentemente después de haber estado sólo unas 24 h en el hospital.
Debido a que muchos pacientes quedan colonizados o infectados con patógenos asociados a las IAAS, puede ocurrir una gran diseminación entre los pacientes a través del contacto directo, por contacto con las superficies ambientales contaminadas o quizás y con mayor frecuencia por las manos contaminadas, ropas o equipamientos de los prestadores de cuidados de salud.
Los prestadores de salud se mueven de paciente a paciente y en ausencia de una adecuada higiene de las manos pueden transmitir fácilmente los patógenos asociados a las IAAS. Se ha demostrado por investigaciones realizadas que, como promedio sólo cumplen las instrucciones de higiene de las manos después del 40 % de los contactos que lo requieren. Las enfermeras y otros profesionales similares lo cumplen con mayor frecuencia que los médicos, pero ninguno alcanza valores superiores al 70 %. Las peores tasas de cumplimiento son observadas en los lugares en que existe mayor riesgo de transmisión, como las unidades de cuidados intensivos, donde están ingresados los pacientes con mayor riesgo de infección y peores pronósticos de sobrevida y que son manipulados con mayor frecuencia y con procedimientos invasivos que favorecen la colonización e infección.
INFECCIONES POR PATÓGENOS RESISTENTES A LOS ANTIBIÓTICOS
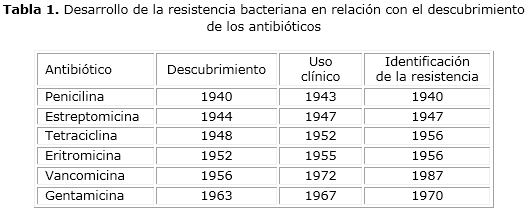
Las infecciones por microorganismos resistentes a los antibióticos se convirtieron en un problema en las instituciones de salud muy pocos años después de la introducción de los antibióticos en la terapia clínica (tabla 1). En ocasiones han sido detectadas sólo pocos meses después de la introducción de nuevas drogas. La resistencia generalmente se identifica primero en los hospitales y después en la comunidad. Algunas resistencias parecen haber aparecido por el uso de suplementos nutricionales en la producción animal como lo es el de la Avoparcina en Europa que provocó la emergencia del Enterococo resistente a la Vancomicina por ser un compuesto relacionado con la Vancomicina.
Estas infecciones son importantes porque se asocian a enfermedad y estadías
hospitalarias prolongadas, riesgo incrementado de muerte y mayor costo a los
sistemas de atención de salud que las infecciones causadas por cepas susceptibles
a los antibióticos de las mismas especies. Han sido identificados dos factores
de riesgo principales para el desarrollo de infecciones por patógenos resistentes
a los antibióticos:
1. El volumen de agentes antimicrobianos (especialmente los de amplio espectro) utilizados en la institución.
2. Diseminación de la infección entre pacientes en una institución (frecuentemente por el personal sanitario).
La razón de la elevada prevalencia de las infecciones nosocomial resistentes
a los antibióticos se explica por la ley de selección natural enunciada
por Charles Robert Darwin, quien advirtió que la naturaleza selecciona
a las especies o cepas mejores adaptadas para sobrevivir en cada medio ambiente.
Debido a que hasta la mitad de los pacientes ingresados en hospitales y casi
la totalidad de los admitidos en unidades de cuidados intensivos reciben antibióticos,
el agente infeccioso que sea resistente a las drogas antimicrobianas administradas
en ese momento tiene una ventaja selectiva para sobrevivir, proliferar y dispersarse.
Para algunas combinaciones de microbios y antibióticos la probabilidad
de que aparezcan mutaciones de resistencia a esa droga particular es tan elevada
que la administración de la misma como monoterapia resulta invariablemente
en la aparición de resistencia antimicrobiana. Los dos mejores ejemplos
son la terapia de las infecciones por el Virus de la Inmunodeficiencia Adquirida
(VIH) y la Tuberculosis. Por ejemplo, la resistencia del Mycobacterium tuberculosis
aparece en el 70 % de los pacientes que reciban monoterapia con Isoniacida
y la monoterapia del VIH resulta invariablemente en la aparición de la
resistencia siempre con cualquier droga antiretroviral. Para otras combinaciones
las probabilidades son inferiores, como por ejemplo las combinaciones del Estreptococo
y la Vancomicina y del Staphylococcus aureus y la Meticillina, que requieren
de la adquisición de determinantes genéticos de resistencia. Más
que de mutaciones espontáneas en el genoma del patógeno.
Por lo tanto el uso amplio e indiscriminado de los antibióticos en conjunto con la transmisión de los agentes infecciosos en forma libre entre los pacientes en las instituciones de salud ha llevado a la emergencia de tasas alarmantes de organismos resistentes a los antimicrobianos, incluyendo a múltiples antibióticos (tabla 2).
ESTRATEGIAS GENERALES EFECTIVAS
EN LA PREVENCIÓN DE LA DISEMINACIÓN DE LA RESISTENCIA EN LOS HOSPITALES
Después de la administración del antibiótico por tan sólo por 7 días se incrementa marcadamente el riesgo de emergencia de la resistencia antimicrobiana. Consecuentemente, su prolongación innecesaria o inadecuada puede seleccionar por aislamientos de gérmenes resistentes a los antibióticos. Tales cepas pueden colonizar y causar infección, así como transmitirse entre los pacientes. Múltiples estudios han documentado una clara relación entre el uso de antimicrobianos y la colonización o infección con organismos resistentes en instituciones de salud, incluyendo una asociación con el uso de drogas de amplio espectro.
El escalonamiento de los antibióticos puede ser una forma más efectiva de prevenir la emergencia de la resistencia en ciertos microorganismos tales como las bacterias gramnegativas, mientras que la prevención de la transmisión pudiese ser más importante para otras como por ejemplo, el Staphylococcus aureus Meticillín-resistente (SAMR).
La higiene adecuada de las manos reduce efectivamente la transmisión nosocomial de gérmenes productores de la IAAS, incluyendo los resistentes. El incumplimiento de sus regulaciones constituye la principal causa de la transmisión de IAAS entre pacientes a través del personal sanitario.
Las manos visiblemente sucias o contaminadas deben ser lavadas con agua y jabón y aquellas que no lo están, deben ser frotadas con una solución alcohólica antes de contactarse a pacientes o realizarse procedimientos clínicos. Asimismo, se deben frotar las manos con esta solución después de haber contactado la piel de un paciente estuviese la misma intacta o no, las mucosas o líquidos corporales. Finalmente, se debe realizar la higiene de las manos después de la retirada de los guantes y el contacto con los objetos inanimados o los equipos médicos en la vecindad del paciente.
Las soluciones alcohólicas han demostrado ser superiores al agua y jabón para la higiene de las manos. Son rápidamente bactericidas y más fáciles de usar, no requieren de un lavamanos, ahorran tiempo y son menos irritantes para la piel que el lavado con agua y jabón. No obstante ello, este último es el método preferido en la prevención de transmisión de la infección en pacientes con afección por Clostridium difficile, ya que las esporas no son eliminadas en forma confiable por el alcohol.
La segregación del personal a través de la dedicación de trabajadores sanitarios dedicados únicamente a brindar cuidados de salud a pacientes conocidos como que están infectados o colonizados por patógenos resistentes ha mostrado un significativo mecanismo de prevención de la transmisión de infecciones por estos agentes, sobre todo en condiciones de brotes. Este personal no puede en ningún momento atender a los pacientes no infectados y viceversa. Se ha demostrado que la insuficiencia de personal contribuye claramente a la diseminación de organismos resistentes, particularmente en condiciones epidémicas, habiéndose demostrado en múltiples estudios una relación estrecha entre este factor, la aglomeración de los pacientes y la diseminación de enfermedades infecciosas.
La reducción de la estancia o frecuencia de ingreso en el hospital, o ambas, así como en las unidades de cuidados intensivos, ha sido sugerida ser un mecanismo efectivo para la reducción del riesgo de la diseminación de organismos resistentes y los resultados de múltiples estudios le dan soporte a esto.
El control de los antimicrobianos en diferentes instituciones no ha dado resultados homogéneos. Por ello algunos han propuesto la identificación acometedora de los pacientes colonizados por microorganismos resistentes4 a través de la realización de escrutinios prospectivos de cultivos a los pacientes y entonces la implementación de medidas de aislamiento y tratamiento para limitar la posibilidad de su transmisión a otros pacientes. Esta medida ha demostrado disminuir la diseminación de patógenos resistentes incluso en ausencia de medidas de control antibiótico, aunque esto probablemente varíe entre microorganismos diferentes. Las limitaciones son la intensiva actividad laboral requerida y su elevado costo y desde el punto de vista práctico, sólo pudiesen ser fijados como meta algunos microorganismos específicos. Por el contrario, esta medida permite identificar patógenos problemáticos rápidamente, antes de que aparezcan brotes de infección y aplicar medidas que impidan su transmisión en el ambiente asistencial. Sin embargo, la eficacia de esta estrategia no ha sido demostrada definitivamente en las investigaciones realizadas debido a su instauración concomitante con otras medidas preventivas.
En Holanda se utiliza un método de búsqueda intensiva para la prevención de la transmisión del SAMR combinado con la restricción de antibióticos a través de la realización de cultivos a toda persona ingresada, combinada con barreras estrictas de aislamiento a las personas identificadas como portadoras del germen, licenciamiento temporal al personal de salud infectado por este germen y cierre de las salas o incluso de instituciones enteras cuando las tasas de infección se elevan. Como ejemplo de la efectividad de estas medidas, la prevalencia de aislamientos del germen ha disminuido a menos del 2 % en todo el país. Similares medidas han sido adoptadas por otros países escandinavos.
La mayoría de las guías para el control de la IAAS recomiendan el aislamiento de los pacientes que hospedan a estos microorganismos y la categoría más utilizada es el aislamiento de contactos. Una descripción de sus resultados informó de una reducción de las tasas de transmisión en 16 veces. A su vez, su aplicación concomitante con otras medidas ha limitado su interpretación más específica. Esta medida tiene consecuencias adversas no intencionadas, como que esos pacientes tienden a tener más complicaciones durante su ingreso y a tener inadecuadas notas evaluativas en sus historias clínicas por parte de sus doctores y enfermeros. También se ha descrito el fallo en la recepción de medidas de soporte, como son la ocurrencia de caídas, aparición de escaras de decúbito y desbalances hidrominerales. Esto parece debido a cambios de actitud y conducta en el personal de atención, por lo cual estos profesionales deben realizar un esfuerzo consciente para asegurar a estos pacientes un nivel de atención adecuado y similar al brindado a los pacientes no aislados.
La rotación o reciclaje de diferentes antibióticos o de sus combinaciones en el tiempo ha sido propuesta como una posible medida de control de la limitación de la aparición de resistencias en las instituciones de salud, aunque hasta ahora sus resultados han sido limitados y hasta contradictorios. Más aún, han sido probados solamente en unidades de cuidados intensivos y no se deberían generalizar a toda la institución de salud. Hasta el momento no existe veredicto final respecto a esta estrategia.
Basados en modelos matemáticos las estrategias que pudiesen reducir en forma efectiva la prevalencia de bacterias resistentes en los hospitales incluyen al control antibiótico, la reducción de la estadía hospitalaria y la instauración de medidas de control de la transmisión de infecciones. Estas últimas incluyen la restricción del contacto entre pacientes y asistentes de salud que sean portadores de bacterias resistentes, mejoramiento de la higiene de las manos y el uso de equipamientos de protección personal como los guantes, máscaras, espejuelos o escudos faciales y gorros. Estos modelos también sugieren que estas intervenciones pueden reducir la transmisión de todo tipo de bacteria dentro del hospital y en una forma muy desproporcionada, reducir la prevalencia de la colonización de bacterias resistentes.
Sin embargo, a un nivel más pragmático, la educación del personal
de salud acerca de la epidemiología, patogénesis y rutas generales
de transmisión de estos gérmenes resistentes, así como el papel
que juega el uso del antibiótico en la emergencia y diseminación de
la resistencia bacteriana resulta de máxima importancia. Se requiere del
conocimiento de estos aspectos por parte del personal de salud tanto para entender
la lógica de las intervenciones como para estimular el cumplimiento de
estas medidas.
CATEGORÍAS DE LA IAAS
INFECCIONES DEL TRACTO URINARIO
Este tipo de infección generalmente sigue a la instrumentación del tracto urinario, mayormente por catéteres. La infección ocurre en el 1 % de los individuos que son cateterizados en una sola ocasión de entrada y salida. En aquellos con prolongación del mismo, el riesgo de infección permanece relativamente constante en el 3 al 6 % por día-catéter. Después de 10 a 14 días de cateterismo cerca de la mitad de los pacientes tienen bacteriuria. Por lo tanto la infección se desarrolla en algún punto en casi todos los pacientes que tienen catéteres permanentes o de larga duración. Las diarreas predisponen a la contaminación del catéter, por lo cual constituyen un factor predisponente independiente. Este tipo de infección constituye entre el 30 y el 40 % de todas las IAAS.
Los patógenos más frecuentemente relacionados son en orden de frecuencias decrecientes: la Escherichia coli, Candida spp, Enterococcus spp, Pseudomona aeruginosa, Klebsiella pneumoniae, Enterobacter spp, Staphylococcus coagulasa negativa, Staphylococcus aureus, Acinetobacter baumanii y Klebsiella oytoca.
Las medidas más recomendadas para su control incluyen el uso del cateterismo urinario sólo para las indicaciones adecuadas y en la duración apropiada, así como la utilización de técnicas de asepsia, inserción y retirada adecuadas, aseguramiento del catéter para evitar su salida y necesaria reinserción y el mantenimiento de la bolsa colectora por debajo del nivel de la vejiga urinaria. Los aditamentos más relacionados con la prevención de la infección son el uso de drenajes cerrados y el uso de catéteres impregnados con antisépticos.
NEUMONÍA
Las vías de infección son a través de la aspiración de los microorganismos en las secreciones de las vías aéreas superiores o del contenido gástrico regurgitado o a través de una diseminación hematógena de una infección a distancia por gérmenes como el Staphylococcus aureus de un catéter venoso central o una fistula arteriovenosa para hemodiálisis. La inhalación directa del germen directamente del aire constituye la tercera vía de infección. Los ejemplos más típicos son el Mycobacterium tuberculosis y el Aspergillus fumigatus. La primera ocurre a través de las microgotas suspendidas en el aire expelidas por la tos de un paciente portador de la enfermedad. Esas microgotas pueden flotar en el aire por horas y pueden infectar a pacientes a una distancia de varias habitaciones. La segunda ocurre por la inhalación de sus esporas que a su vez son liberadas de la superficie de cualquier material orgánico, en el cual puede crecer (por ejemplo, una naranja). La inhalación de estas esporas se incrementa cuando hay labores de construcción o demolición. La aspiración a partir del agua potable es otro mecanismo posible, como ocurre en la infección por Legionella.
La mayoría de los pacientes que adquieren la neumonía nosocomial han sido mantenidos en ventilación mecánica en una unidad de cuidados intensivos.5 Los agentes causales más frecuentes son (por orden decreciente): Staphylococcus aureus, Pseudomonas aeruginosa, Enterobacter spp., Acinetobacter baumannii, Klebsiella pneumoniae, y la Escherichia coli.
La neumonía asociada a la ventilación mecánica (NAV) varía en el rango del 6 al 30 % con un riesgo del 1 al 3 % por día de intubación y ventilación mecánica. En los pacientes críticos en ventilación mecánica en posición supina el pool de secreciones orofaríngeas y en el espacio subglótico por encima del cuff del tubo endotraqueal constituyen un reservorio de secreciones contaminadas que frecuentemente son aspiradas a los pulmones vía las paredes del tubo. La utilización de un dispositivo que succione continuamente dichas secreciones ha sido asociada a una reducción de la aspiración clínica de estas secreciones y un menor desarrollo de la NAV, que se define como la neumonía que comienza entre el tercer y el quinto día después de la intubación.
La luz interior del tubo endotraqueal se cubre rápidamente de una biocapa que contiene grandes concentraciones de microorganismos. Porciones de esta biocapa pueden ser inoculadas directamente en el tracto respiratorio inferior, ya sea por el flujo ventilatorio o por la inserción de dispositivos a través del tubo (como durante la aspiración o la realización de una broncoscopía). Estas porciones de la biocapa pueden sembrarse en el parénquima pulmonar y servir como nido para la infección en progreso.
La utilización de la nutrición enteral intermitente o continua provoca elevación del PH gástrico disminuyendo su poder antibacteriano. Lo mismo ocurre con el uso de antiácidos potentes, por lo que incrementa el riesgo de la infección debido al sobrecrecimiento bacteriano en el lago gástrico. Cuando estos líquidos son regurgitados y aspirados, se desarrolla rápidamente una neumonía debido al gran inóculo infeccioso aportado. El uso del sucralfato, que no disminuye el PH gástrico en la prevención de las úlceras de estrés durante la ventilación mecánica ha sido asociado a menores tasas de neumonía nosocomial en algunos estudios. No obstante ello, otros estudios han sugerido que este medicamento puede que no sea tan efectivo como otros en la prevención del sangramiento digestivo.
La aspiración del contenido gástrico ocurre 4 veces más frecuentemente cuando el paciente se encuentra en la posición supina en relación a cuando su cabeza está elevada en un ángulo de 45 grados. No obstante ello, en los pacientes ventilados con intubación gástrica, ocurre frecuentemente el reflujo gástrico independientemente de la posición en el lecho. Las recomendaciones actuales para la prevención de la NAV incluyen la elevación de la cabeza entre 30 y 40 grados a menos que exista contraindicación médica por otras razones.
La descontaminación antibiótica selectiva del tracto digestivo también ha demostrado resultados favorables en la reducción de las tasas de NAV y mortalidad, pero trae aparejada la aparición rápida de resistencia por parte de la flora gastrointestinal. No obstante, la higiene adecuada de la cavidad oral ayuda en la prevención de la NAV sin el riesgo de la introducción de la resistencia bacteriana.
INFECCIÓN DEL SITIO QUIRÚRGICO
Los gérmenes más comúnmente involucrados en este tipo de infección en orden decreciente son el Staphylococcus aureus, el Staphylococcus coagulasa negativa; Enterococcus spp, los bacilos gramnegativos tales como la Escherichia coli, Pseudomona aeruginosa, Enterobacter spp, Klebsiella spp, y el Acinetobacter baumannii, y finalmente la Candida spp.6
Actualmente este tipo de IAAS depende más de la habilidad quirúrgica del cirujano y de la existencia de condiciones preexistentes en el paciente.
Esta complicación anteriormente era casi inevitable en los medios hospitalarios, pero actualmente esto se ha revertido para los procederes “limpios”.7 La mayoría de estos procederes se realizan cumpliendo normas de asepsia que impiden la contaminación del lecho quirúrgico como son la asepsia de las manos del cirujano y de la piel del paciente, el uso de barreras estériles (gorros y guantes quirúrgicos), la profilaxis antibiótica prequirúrgica y cuando sea apropiada, continuada con dosis adicionales del antibiótico durante la operación, así como la esterilización del instrumental quirúrgico.
Hay una gran variedad de factores relacionados con la pericia quirúrgica entre los cuales se pueden mencionar la presencia de espacio muerto y de tejido necrótico en la herida (como suele suceder con el uso excesivo de la electrofulguración), el afeitado de la piel el día previo a la operación, lo cual debe ser sustituido por la remoción del pelo con máquinas eléctricas una hora antes.
La administración de la profilaxis antibiótica debe ser dentro de la primera hora antes del momento de la incisión quirúrgica para asegurarse niveles adecuados de la droga y deben ser administradas nuevas dosis si el procedimiento se prolonga más de 4 h. Finalmente el antibiótico no debe ser utilizado por más de 24 h después del procedimiento y frecuentemente no son necesarios con posterioridad al evento quirúrgico. Los pacientes con heridas quirúrgicas contaminadas en forma intrínseca (por ejemplo, la ruptura apendicular) tienen una mayor probabilidad de riesgo de infección a pesar de las medidas preventivas modernas debido al gran inóculo bacteriano y a que la infección puede haber estado ya presente en el momento de la intervención. La descontaminación intestinal antes de la cirugía persiste como una importante y efectiva opción para la reducción del riesgo de desarrollo de la IAAS. Por ejemplo, la cirugía del colon después de la profilaxis antibiótica y limpieza mecánica durante el proceder se asocia a tasas inferiores de infección.
Los factores relacionados con el paciente son la obesidad, la Diabetes Mellitus, y la enfermedad vascular periférica severa.
El control de los niveles de glicemia, el mantenimiento de la normotermia durante el tiempo quirúrgico, el escrutinio de la colonización por el Staphylococcus aureus antes de la operación y su adecuada descontaminación a través de los baños y duchas con jabón bactericida (por ejemplo con Clorhexidina) han reducido las tasas de infección del sitio quirúrgico. Sin embargo, la interpretación adecuada de estas evidencias está afectada también por el hecho de la introducción simultánea de otras medidas de control de las IAAS. Finalmente se debe mencionar el papel de la reducción de la infección quirúrgica a través de la información al personal quirúrgico de las complicaciones infecciosas postquirúrgicas.
INFECCIONES DEL TORRENTE SANGUÍNEO
Estas pueden ocurrir después de la infección primaria del sistema cardiovascular, generalmente después de la inserción de un catéter intravascular,8,9 o pueden ser secundarias a una infección local en otro órgano. Aproximadamente el 80 % de las IAAS del torrente sanguíneo son primarias y debidas a catéteres y el 20 % son secundarias a infecciones en otros órganos.
Los gérmenes causales en orden decreciente de frecuencias son los Staphylococcus coagulasa negativa, Enterococcus spp, Candida spp, Staphylococcus aureus y los bacilos gramnegativos tales como la Klebsiella pneumoniae y el Enterobacter spp. Aunque definitivamente los Staphylococcus coagulasa negativa causan este tipo de infecciones, la mayoría de los cultivos que muestran este germen en realidad constituyen contaminaciones y no verdaderamente infecciones. Por el contrario, el Staphylococcus aureus y la Candida spp son más virulentos y se asocian con una mayor probabilidad a ser verdaderas infecciones del torrente sanguíneo.
Los microorganismos pueden alcanzar la circulación por tres vías separadas asociadas al uso de catéteres endovenosos. Estos pueden colonizar el sitio de inserción del catéter y subsecuentemente moverse a través de los tejidos, pueden colonizar los dispositivos asociados al catéter como las llaves de tres pasos, uniones, y otros conectores y ganar por este medio el acceso al sistema endovascular cuando estos sitios son manipulados, así como a través de contaminación intrínseca o extrínseca del líquido de infusión.
Este tipo de infección generalmente comienza con la colonización del catéter. Puesto que estos generalmente son insertados a través de la piel del paciente muchos de tales microbios provienen de la flora bacteriana de la piel. La contaminación del catéter es universal durante el primer día después de la inserción.
Los microorganismos migran a través del tracto de inserción por acción capilar y la colonización suele ocurrir en el momento de la inserción, pero puede ocurrir días después. Inicialmente la colonización ocurre en la cara externa del catéter. Por el contrario, los estudios ultraestructurales han demostrado la existencia de una frecuencia elevada de contaminación intraluminal ya para el décimo día de la inserción, por lo que parece ser que la mayoría de los catéteres de inserción prolongada son colonizados y producen infección del torrente sanguíneo a través de la vía intraluminal. La colonización está facilitada por la formación de una capa de fibrina alrededor del catéter como resultado de la deposición de plaquetas y también está facilitada por la formación de una biocapa de microorganismos.
Una estrategia eficiente para reducir los riesgos de infección es el uso de antisépticos para la limpieza de la piel antes de la inserción del catéter y continuar después con su aplicación cada pocos días después para la reducción de la carga microbiológica. En múltiples estudios la Clorhexidina ha mostrado superioridad a las soluciones de alcohol y de Iodo povidona en la prevención de esta infección.10 También deben ser utilizadas barreras de protección máxima para crear campos extensos de esterilidad durante la inserción del catéter, lo que ha demostrado tener gran efectividad.11
Existe otro gran número de factores que intervienen en la reducción del riego, como el tipo de vendaje, la composición del catéter, el número de luces del catéter y el tipo del sistema de administración intravenosa utilizado. Tanto los vendajes con algodón como los de gasa cubiertos con esparadrapo o con membranas transparentes semipermeables pueden ser utilizados para la protección del sitio de inserción, pero a pesar de ello, la carga microbiana cutánea se incrementa sustancialmente por debajo del vendaje semipermeable. Por el contrario, este último requiere de menor frecuencia de cambios y manipulaciones y asegura el anclaje del dispositivo con mayor seguridad que los vendajes de gasa y esparadrapo. Sin embargo, ambos tipos de vendajes han mostrado similares tasas de infección y complicaciones locales. El uso de vendajes impregnados en Clorhexidina ha reducido las tasas de infección también, así como el uso de diferentes tipos de catéteres. Por ejemplo, los catéteres realizados con material rígido traumatizan el endotelio vascular y se mueven alrededor del sitio de inserción, favoreciendo el incremento del riesgo de la colonización e infección. Y finalmente se debe mencionar que la manera en que son utilizados los catéteres puede influenciar dicho riesgo. Por ejemplo, en los pacientes críticos los catéteres pulmonares son reposicionados con frecuencia para la obtención de mediciones confiables provocando traumatismos endoteliales locales.
Los factores relacionados con los procederes de salud también están involucrados en el riesgo. Por ejemplo, el lavado de las manos, la manipulación de los sistemas de administración intravasculares, por ejemplo para la reposición del catéter, la colección de muestras de sangre, la administración de medicamentos, también favorece la probabilidad de la colonización. La técnica de inserción y mantenimiento también influencian esto. El sitio de inserción también influye. El abordaje por vía femoral se asocia a tasas superiores de infección.
Una de las medidas dirigidas a limitar este tipo de IAAS ha sido la utilización de catéteres impregnados en sustancias antimicrobianas ya sean antibióticas o antisépticas. Un catéter impregnado en Clothexidina y Sulfadiazina de plata ha logrado reducir la tasa de infección en un 50 % y catéteres impregnados de minociclina y rifampicina los han logrado en magnitudes aún mayores. También son superiores aquellos que están impregnados tanto por el exterior como por el interior. Sin embargo, esto implica el riesgo de desarrollo de resistencia antimicrobiana a estos agentes, aunque no ha sido demostrado aún.
Se encuentra en estudio la utilización de sistemas de administración de líquidos sin agujas, pero los resultados han sido contradictorios, posiblemente por el no seguimiento de las recomendaciones del fabricante debido a su desconocimiento por el personal.
Se han propuesto cinco medidas importantes en el control de este tipo de infección. Estas son la higiene de las manos con técnicas adecuadas, la utilización de precauciones máximas barreras durante la inserción, la antisepsia cutánea con Clorhexidina la selección óptima del sitio de inserción y la revisión diaria de la necesidad del mantenimiento del catéter con pronta remoción una vez no sea necesitado más.12
OTRAS INFECCIONES NOSOCOMIALES
Aproximadamente el 6 % de las infecciones nosocomiales no ocurren en ninguna de estas cuatro localizaciones previamente abordadas. Actualmente el 25 % son de tipo misceláneo. Estas incluyen las infecciones gastrointestinales por el Clostridium difficile, rotavirus, y Salmonella spp. También se incluyen las infecciones virales por varicela, influenza, y el virus sincitial respiratorio, así como las infecciones orales, esofágicas y vaginales por cándida.
REFERENCIAS BIBLIOGRÁFICAS
1. Kelly MJ. Hospital-acquired infections. Surgery. 2012;30(12):640-4.
8. Martinez-Morel HR, Sanchez-Paya J, Molina-Gomez MJ, Garcia-Shimizu P, Garcia Roman V, Villanueva-Ruiz C, et al. Catheter-related bloodstream infection: burden of disease in a tertiary hospital. The Journal of hospital infection. 2014;87(3):165-70. Epub 2014/06/15.
12. Dumyati G, Concannon C, van Wijngaarden
E, Love TM, Graman P, Pettis AM, et al. Sustained reduction of central line-associated
bloodstream infections outside the intensive care unit with a multimodal intervention
focusing on central line maintenance. American journal of infection control.
2014;42(7):723-30. Epub 2014/05/27.
Recibido: 28 de marzo de 2015.
Aprobado: 28 de abril de 2015.
Liodelvio Martínez Fernández.
Servicio de Medicina Interna. Hospital Clínico Quirúrgico Hermanos
Ameijeiras. La Habana. Cuba.
Correo electrónico: liodelvio@infomed.sld.cu